美股上市药企分析—CRISPR Therapeutics
$CRISPR Therapeutics AG(CRSP)$
转自微信公众号:换汤不换药
前言
2020年诺贝尔化学奖又一次颁给了生命科学领域,来自法国的科学家埃马纽埃尔·卡彭蒂耶(Emmanuelle Charpentier)和来自美国的科学家珍妮弗·安妮·道德纳(Jennifer A. Doudna)发现了基因技术中最锐利的工具之一:CRISPR/Cas9“基因剪刀”,基于这项技术,研究人员可以极其精确地改变动物、植物和微生物的DNA。2013年,Emmanuelle和其合伙人在波士顿创办了CRISPR Therapeutics,公司主要研究CRISPR-Cas9基因编辑技术及其在β地中海贫血、血友病、杜氏肌营养不良症、囊性纤维化等疾病治疗中的应用。下面将对CRISPR Therapeutics进行详细的介绍。
01 基本面分析
1.1 公司基本介绍
CRISPR Therapeutics于2013年成立,总部位于瑞士巴塞尔,在美国马萨诸塞州剑桥市开展研发业务,公司专注开发基于CRISPR/Cas9技术的基因编辑治疗药物,其技术可以对基因组DNA进行精确、定向的改变,可以用于β地中海贫血、血友病、杜氏肌营养不良症、囊性纤维化等疾病的治疗。公司于2016年10月19日在纳斯达克上市,发行价为15美元,上市时市值为5.9亿美元 。
1.2 公司技术介绍
CRISPR全称为成簇规律间隔短回文重复序列系统技术(Clusteredregularly interspaced short palindromic repeats),又称为CRISPR/Cas系统,是原核生物的一种天然免疫系统。 某些细菌在遭到病毒入侵后,能够把病毒基因的一小段存储到自身的DNA 中一个称为CRISPR的存储空间。 当再次遇到病毒入侵时,细菌能够根据存写的片段识别病毒,将病毒的DNA切断而使之失效。
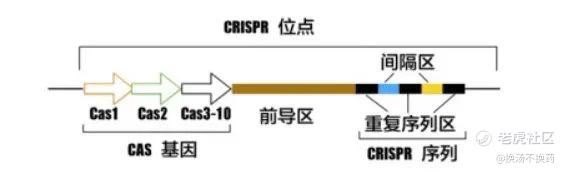
CRISPR的作用机制:CRISPR/Cas系统由CRISPR和Cas核酸酶组成。CRISPR基因序列主要由前导序列(leader)、重复序列(repeat)和间隔序列(spacer)构成,该系统的前导区负责启动转录开始并合成前 CRISPR-RNA(该段序列负责与DNA配对,并提供模版)。现在的基因工程中常用的Cas核酸酶是Cas9核酸酶,该酶负责切割DNA。Cas9酶有2 个重要的核酸酶结构域,分别是RuvC 和HNH结构域(可以理解为是一种识别工具)。HNH 结构域负责断裂通过互补靶向的DNA单链,切割位点位于PAM序列(可以理解为是一种标记物)上游3个碱基处。
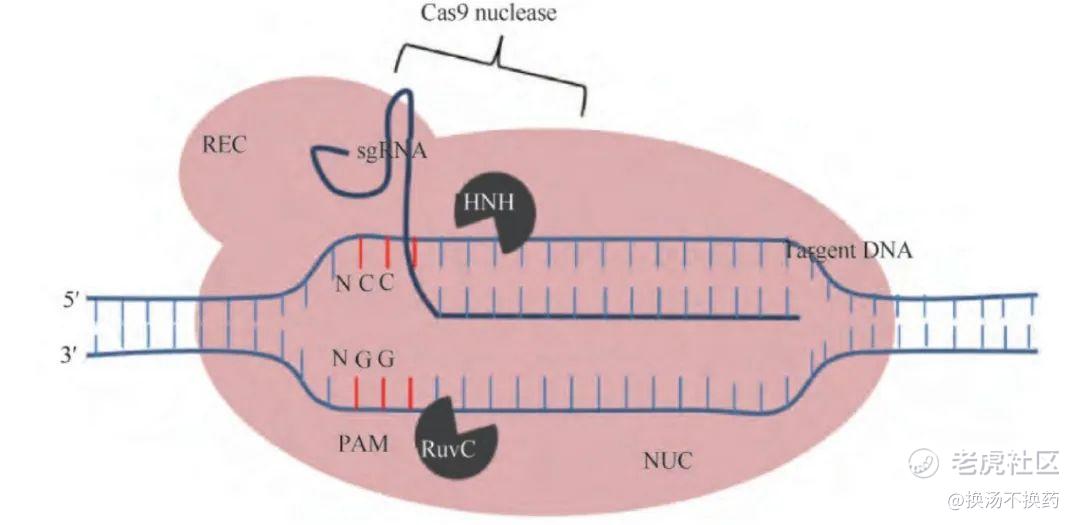
CRISPR-Cas9 基因编辑技术就是通过人工设计的 sgRNA(guide RNA)来识别目的基因组序列,并引导Cas9蛋白酶对DNA 双链进行有效切割,形成双链断裂,断裂后的修复会造成基因沉默、敲除或敲入等,从而达到对基因组DNA进行修饰的目的。 CRISPR-Cas9基因编辑技术属于第三代基因编辑技术,能够同时实现多个基因的编辑,靶向效率更高,并且操作简单,构建成本低 。
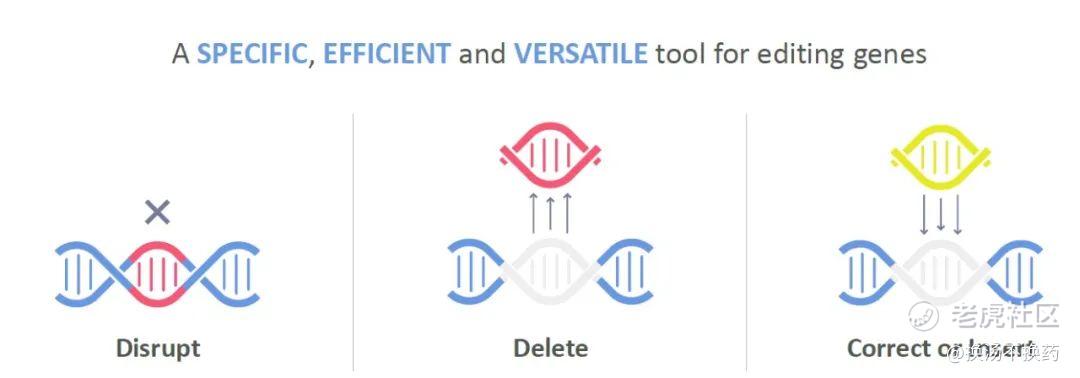
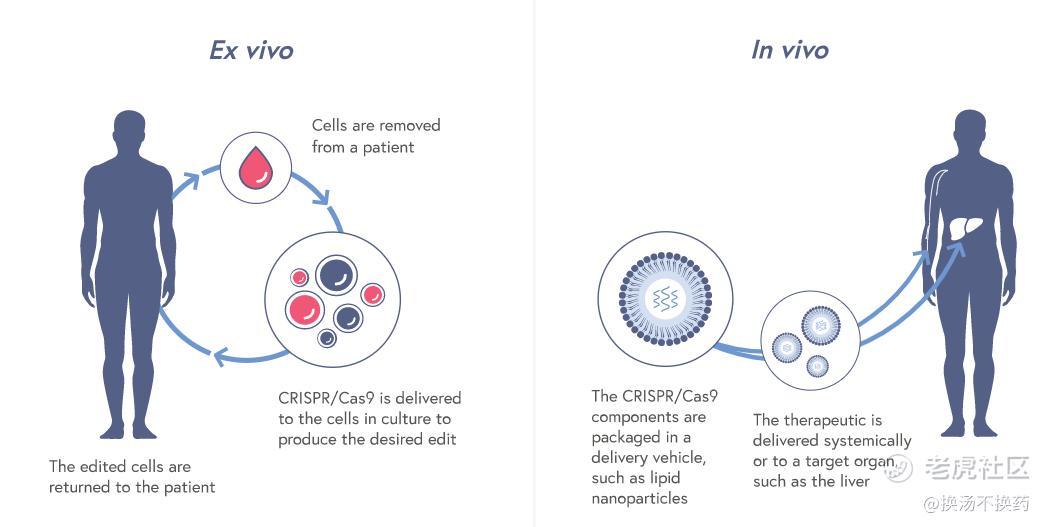
目前CRISPR/Cas9系统主要分为体外和体内两种应用。 针对体外的应用主要以纯化的 Cas9核酸酶配以向导RNA,用于在体外对基因组片段进行靶向切割以替代传统的限制性内切酶或PCR克隆。 针对体内的应用主要是以载体的形式将Cas9和向导RNA送入细胞,在体内表达和转录后发挥作用 。
1.3 研发管线
CRISPR Therapeutic根据一系列标准选择适应症和靶点,建立起一套产品组合: 具体包括未满足的医疗需求、技术可行性、CRISPR/Cas9相对于其他方法的优势以及将候选产品推进到临床试验所需的时间等。

血红蛋白病(Hemoglobinopathies)是一组在世界范围内广泛流行的单基因遗传性血液病。 其中β-地中海贫血和镰状细胞病(SCD)是由β珠蛋白基因突变引起的,该基因编码血红蛋白的一个关键成分,即血液中的携氧分子。 这两种疾病目前都需要终生治疗,这导致患者出现疼痛症状,并需要定期输血和长期住院治疗。 这两种疾病都将导致预期寿命缩短 。
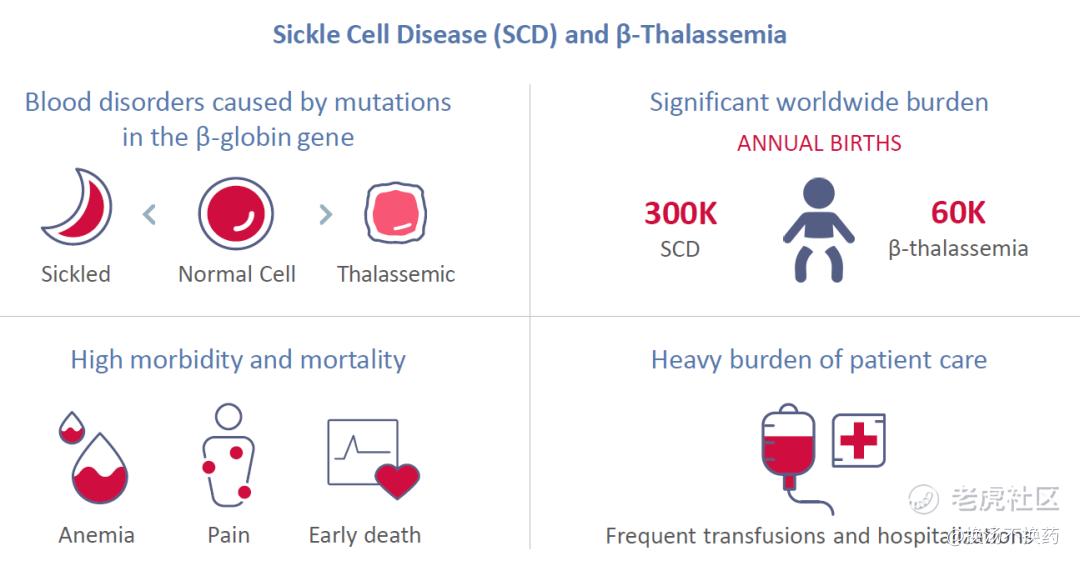
CTX001是CRISPR与福泰制药公司(Vertex Pharmaceuticals)合作的一种自体的、体外CRISPR/Cas9基因编辑的造血干细胞疗法,目前正在评估用于治疗输血依赖性β-地中海贫血(TDT)和重度镰状细胞病(SCD)的1/2期临床研究,是全球第一个达到人体阶段测试的基于CRISPR/Cas9的基因编辑疗法。 在这种疗法中,患者的造血干细胞被改造成在红血球中产生高水平的胎儿血红蛋白(HbF,血红蛋白F)。 HbF是一种携带氧气的血红蛋白,在出生时自然存在,然后转换为成人形式的血红蛋白。 CTX001使HbF升高可以减少TDT患者的输血需求,减轻SCD患者的痛苦和会让人变得虚弱的镰状细胞现象。
TDT患者 平均每年需要输血16.5次,在CRISPR披露的两名患者的临床试验数据中,在接受一次性CTX001治疗2个月后,均完全摆脱了对于输血的依赖,且表现出了强劲、持久的HbF表达。
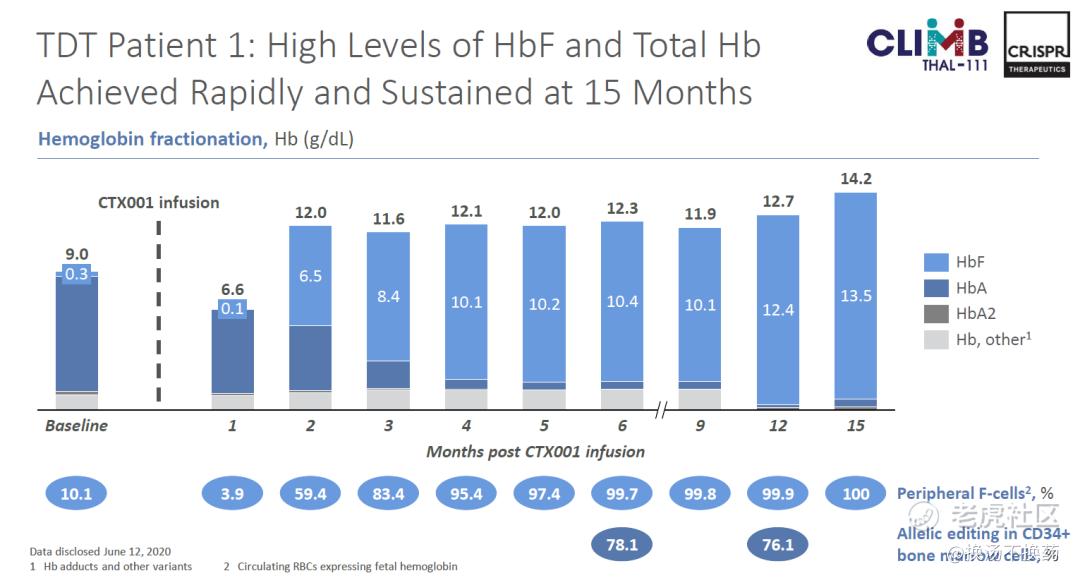
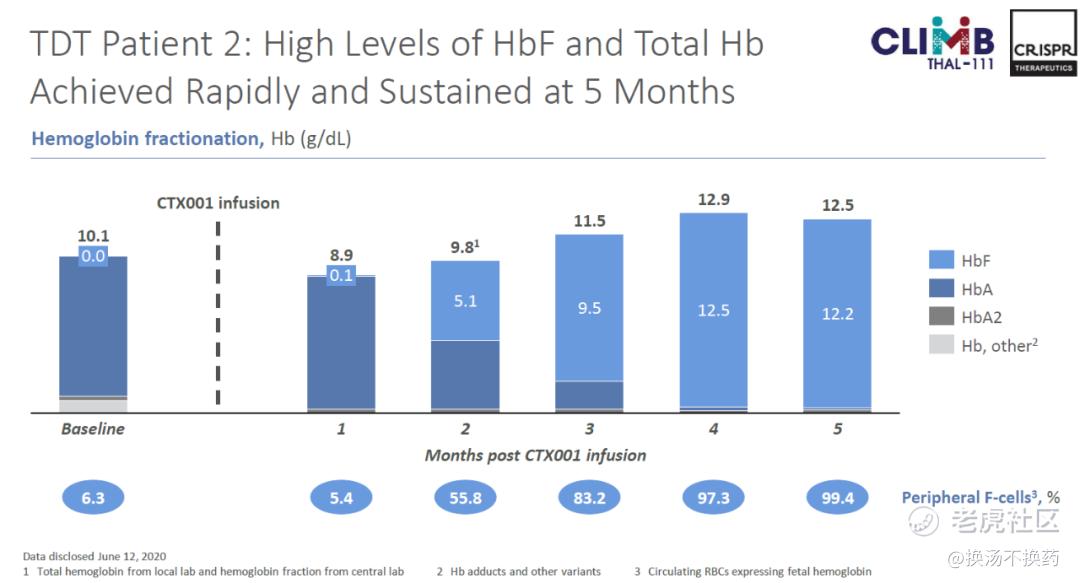
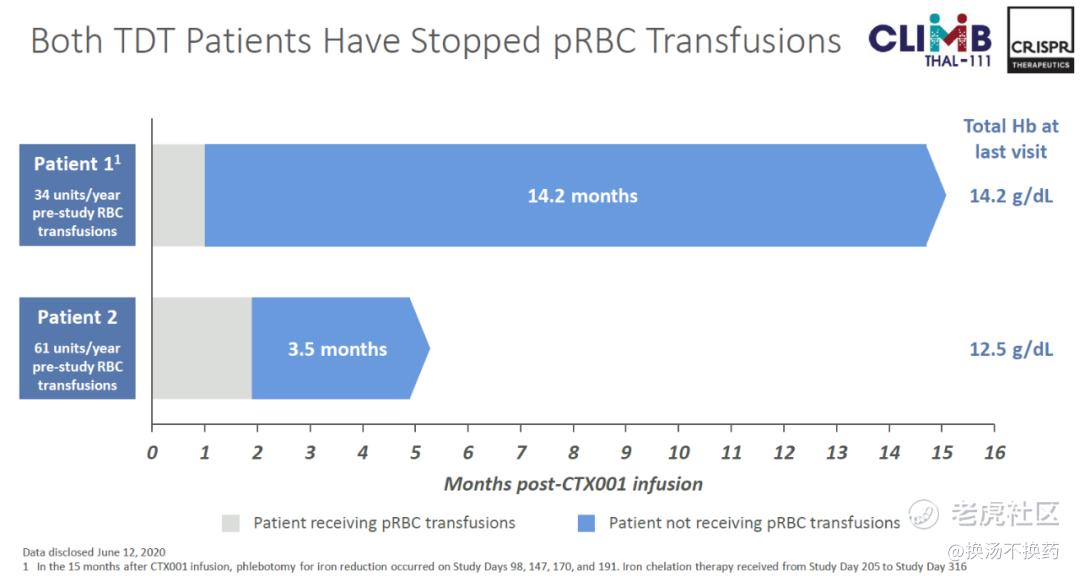
在SCD的临床试验中,患者此前每年平均发生7次血管堵塞(血管闭塞危机),但在治疗的9个月期间,患者没有发生过1次堵塞。 并且同样在单剂量输注CTX001后,患者体内快速实现了强劲、持久、泛细胞HbF高水平表达。
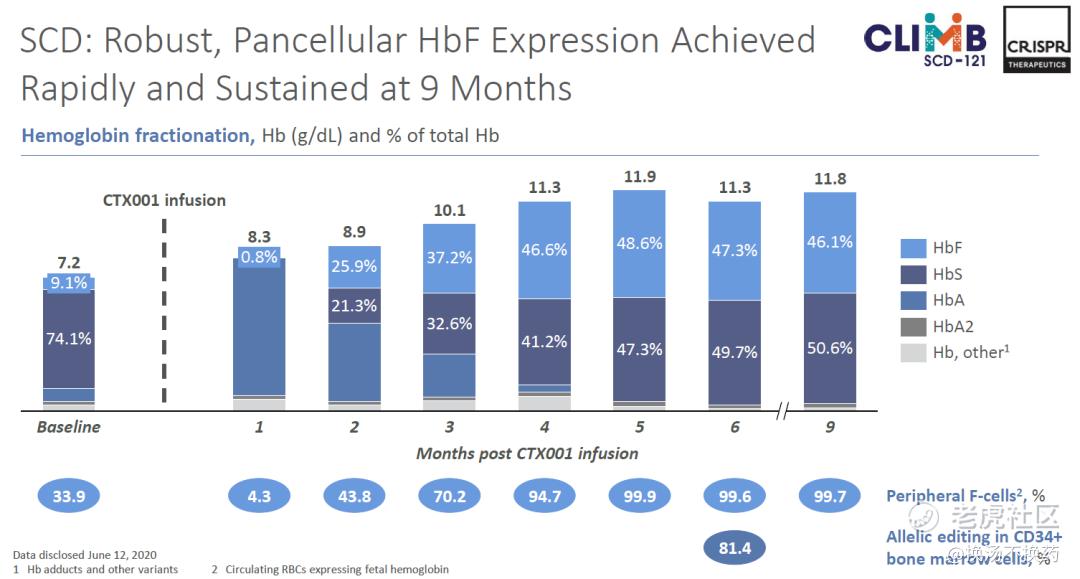
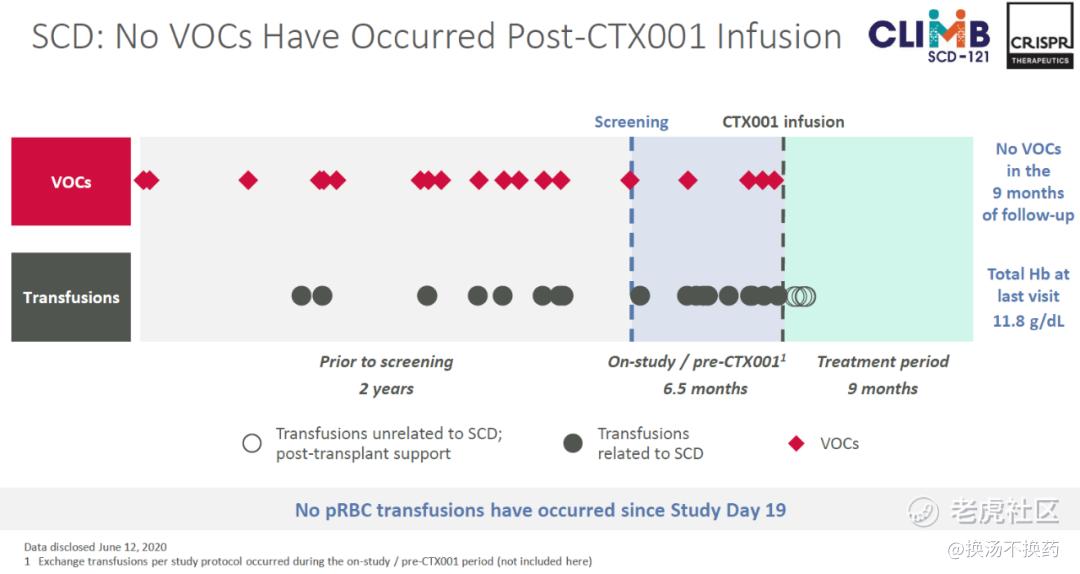
在肿瘤免疫治疗领域,CRISPR主要专注于异体CAR-T,使其成为所谓的off-the-shelf(即用型产品)新一代CAR-T。
在产品CTX110中,首先将CD19嵌合抗原受体或CAR插入到特定选择的基因座中,然后消除T细胞受体(TCR),以便能够在不同的患者中使用同一批次产品。 最后,消除1类主要组织相容性复合体(MHC I)以改善CAR-T细胞的耐久性。 多个基因编辑可以同时完成。
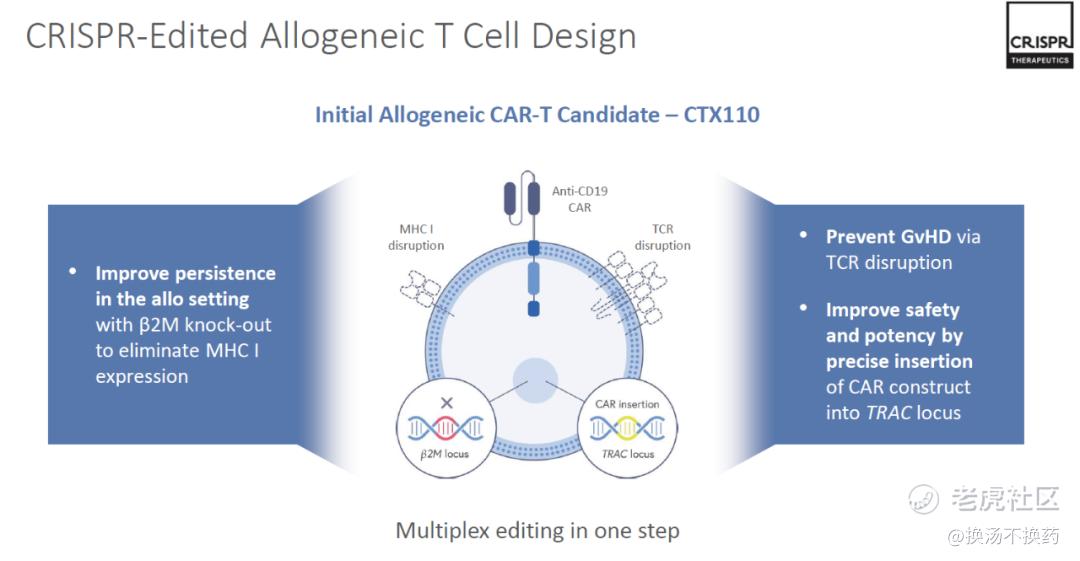
CRISPR目前3款异体CAR-T产品分别为CTX110(靶点为CD19: B细胞系肿瘤)、CTX120(靶点为BAMA: 多发性骨髓瘤等)、CTX130(靶点为CD70: 胶质母细胞瘤等),在动物试验中均取得良好的数据。
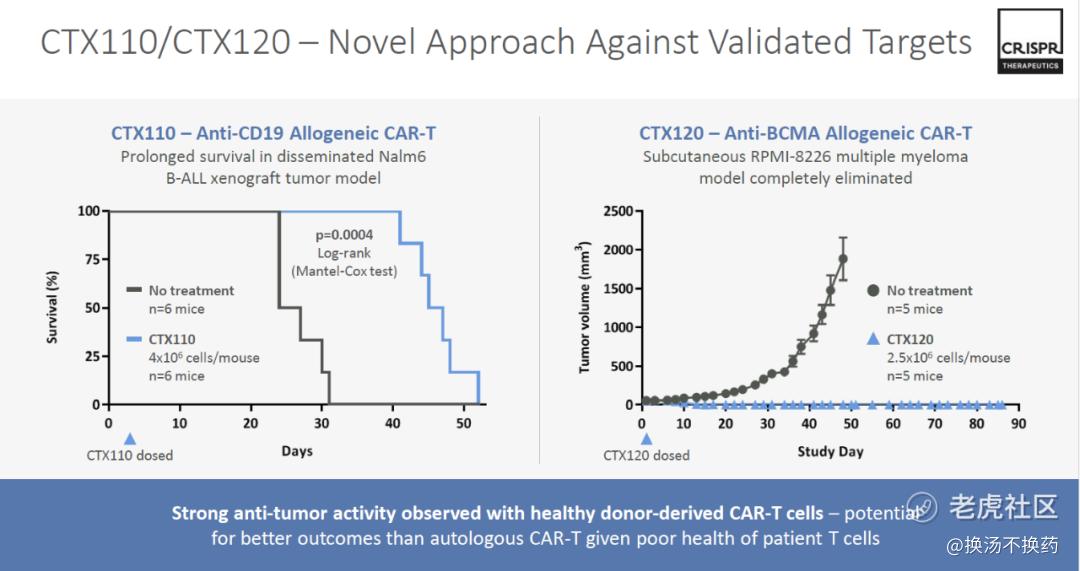
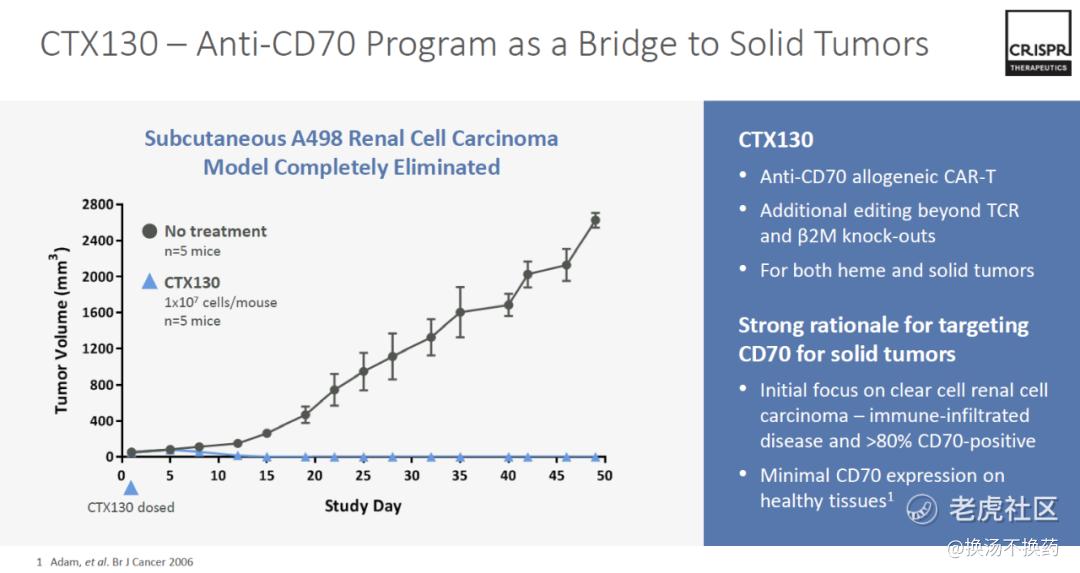
在再生医学和体内基因编辑两个方向,目前CRISPR仍处于早期研发中,基于CRISPR/Cas9基因编辑疗法力的巨大潜力,I型糖尿病、杜氏肌营养不良症(DMD)等罕见病有望从根本上得到治疗 。
02 资本市场
2.1 融资情况
据公开信息统计,CRISPR在一级市场总共筹集了1.27亿美元,早期 投资方为Versant Ventures。
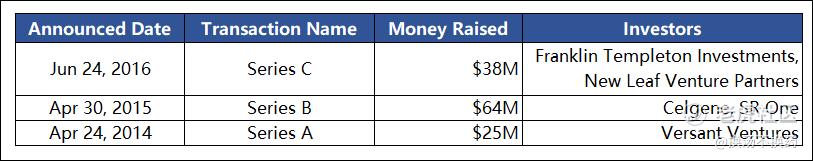
Versant Ventures是一家全球领先的医疗保健投资公司,致力于帮助杰出企业家打造下一代伟大的医疗保健公司。公司投资于医疗保健行业和公司发展的各个阶段,重点在于发现和开发新的疗法。Versant Ventures管理着30亿美元的资产,自1999年公司成立以来,已有超过65家Versant投资的公司被成功收购或IPO。
2.2 财务情况
截至目前,Versant Ventures仍是CRISPR的最大机构投资方。
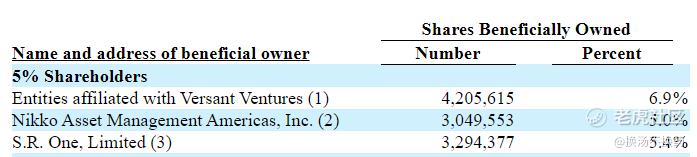
截至2020年6月30日,CRISPR账上现金为9.45亿美元,资金充足,净资产超过9亿美元,财务状况非常好。
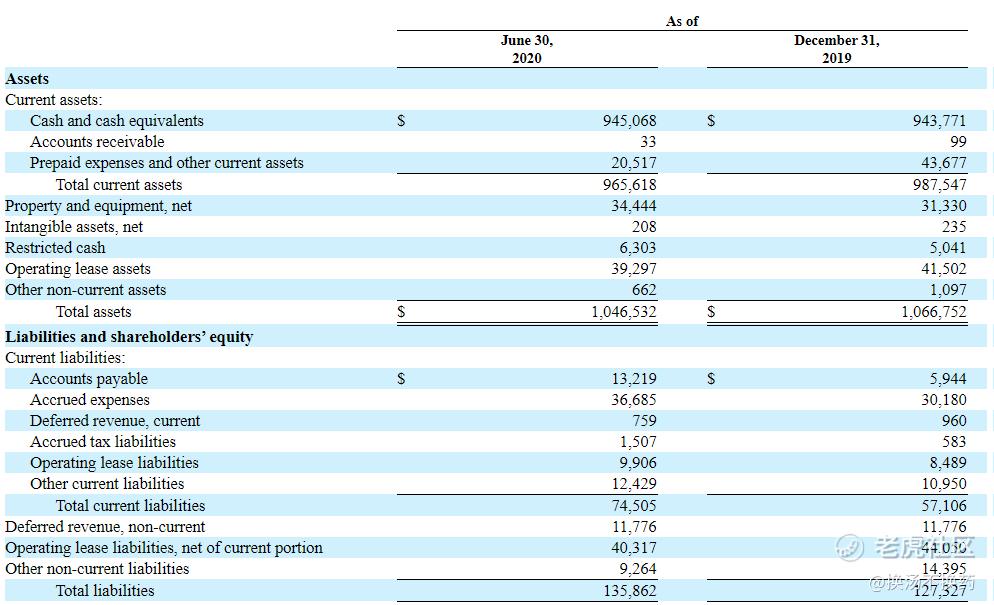
03 小结
诺贝尔化学奖颁布当天,CRISPR股票大涨11%,目前仍是基因编辑领域市值最高的公司。诺奖的热度,加上公司产品管线的积极试验结果,以及CRISPR/Cas9基因编辑疗法自身的巨大潜力,CRISPR将在相当长的一段时间内作为市场上最佳的基因编辑概念股。
免责声明:上述内容仅代表发帖人个人观点,不构成本平台的任何投资建议。



