医药观澜:艾力斯超1.8亿美元引进,可穿越血脑屏障,肺癌1类新药获批临床
医药观澜
▎药明康德内容团队报道
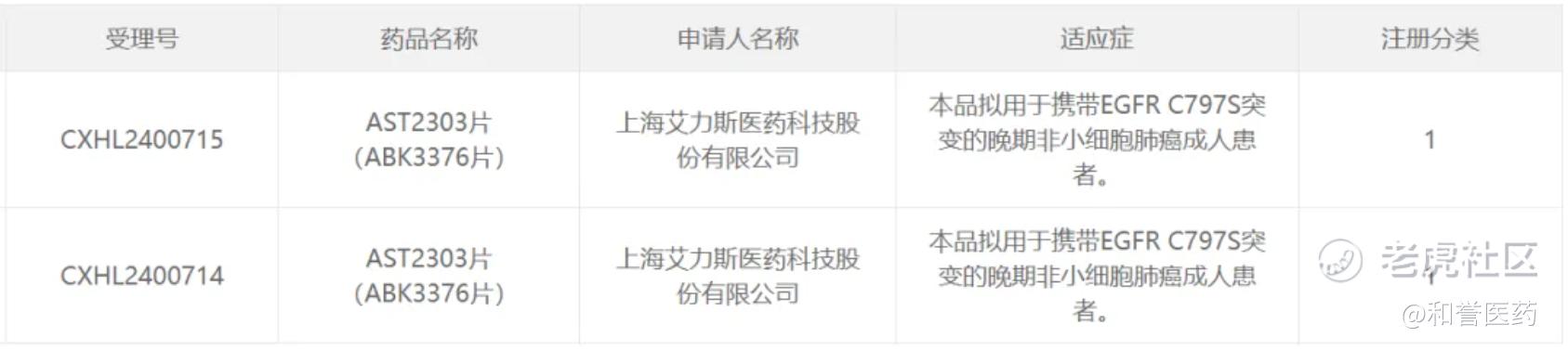
今日(9月23日),中国国家药监局药品审评中心(CDE)官网刚刚公示,艾力斯医药申报的AST2303片(ABK3376片)获批临床,该产品拟用于携带EGFR C797S突变的晚期非小细胞肺癌成人患者。公开资料显示,这是一款新一代小分子表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)。2023年10月,艾力斯医药与和誉医药达成一项约1.879亿美元的合作,获得该产品在中国(包括中国大陆、香港、澳门和台湾地区)的研究、开发、制造、使用以及销售的独家许可。
当前,第三代EGFR-TKI已成为临床上肺癌治疗的常规用药,但耐药的发生仍然难以避免。其中,C797S是肺癌靶向治疗中极为常见的靶向耐药机制。
根据和誉医药和艾力斯医药此前公开资料,AST2303是一款高选择性、可入脑的新一代EGFR口服小分子抑制剂,可高效抑制三代EGFR-TKI耐药后产生的C797S突变。临床前的研究结果显示,AST2303具有较好的肿瘤细胞抑制和杀伤活性,以及对野生型EGFR较高的选择性,从而具有较好的安全性。
此外,AST2303还具有高效穿透血脑屏障的特性,可在中枢神经系统(CNS)获得有效的药物暴露,有望用于治疗或预防非小细胞肺癌的CNS转移。研究表明,在有基线脑转移的EGFR突变非小细胞肺癌患者中,多达40%的疾病进展涉及CNS转移。
临床前研究还显示,AST2303无论单药还是与艾力斯已上市的第三代EGFR抑制剂伏美替尼联用,都取得了积极的结果,有望成为精准治疗伴有EGFR-C797S耐药突变非小细胞肺癌的新一代靶向治疗药物。
艾力斯医药专注于肿瘤治疗领域,该公司核心产品第三代EGFR-TKI伏美替尼已经在中国获批两项肺癌适应症,目前还在多个不同的非小细胞肺癌类型中进行临床探索,比如与和誉医药联合开展口服PD-L1小分子药物联合用药治疗晚期非小细胞肺癌等等。此外,该公司还在不断丰富产品管线,其自主研发的KRAS G12D选择性抑制剂注射用AST2169脂质体已经于今年3月获批临床。
本次这款第三代EGFR-TKI产品获批临床,意味着艾力斯医药又一款创新药进入临床研发阶段。
免责声明:上述内容仅代表发帖人个人观点,不构成本平台的任何投资建议。