Cell Biosci|张敬法教授团队:从细胞和分子角度探讨微血管不稳定和细胞因子复杂网络在糖尿病视网膜病变中的作用
编者按
微血管不稳定是糖尿病视网膜病变(DR)血-视网膜内屏障(iBRB)破坏和血管渗漏增加的主要原因。微血管不稳定是由视网膜中各种生长因子和细胞因子水平升高、炎症参与以及细胞间相互作用改变等综合因素所导致。随着微血管不稳定的加剧,视网膜血管内皮细胞间连接复合体破坏和/或跨血管内皮转运的改变,通过细胞旁和跨细胞途径的液体转运增加,血管渗漏加剧、水肿加重。而随着糖尿病进展,iBRB组分(包括细胞和非细胞组分)的功能和结构变化进一步加重了微血管不稳定,导致黄斑水肿加重、神经视网膜损伤和视网膜神经血管内单元(iNVU)功能障碍。尽管近年来导致微血管不稳定的研究取得了巨大进展,但仍有许多问题尚待阐明。近日,香港中文大学(深圳)国际眼科研究所、希玛眼科张敬法教授团队发表了题为“Microvascular destabilization and intricated network of the cytokines in diabetic retinopathy: from the perspective of cellular and molecular components”的综述,旨在通过靶向关键分子或特定的iBRB细胞,恢复iBRB和iNVU的功能和结构,进而治疗DR,为微血管不稳定提供深入见解。该综述已被“Cell Biosci. (IF 6.1)”接收并在线发表。
DR与微血管不稳定
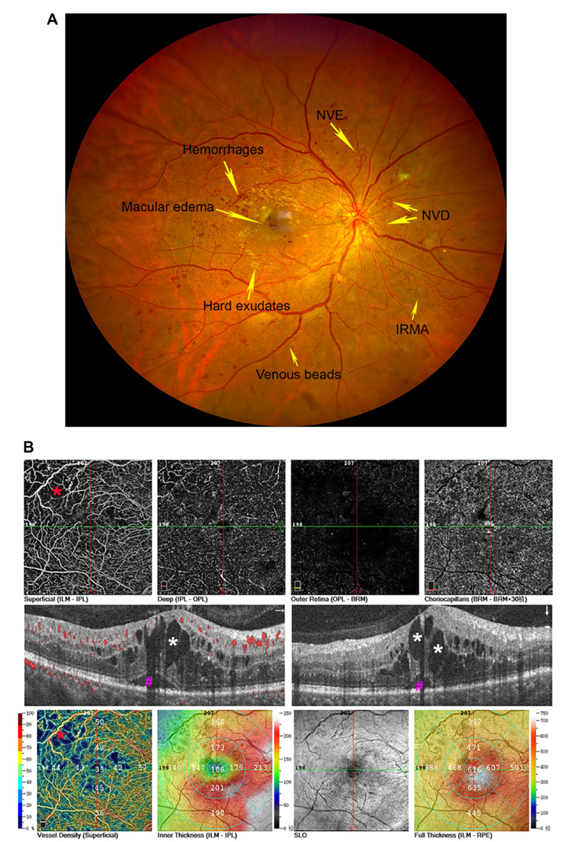
DR主要基于高血糖引起的微血管变化,分为非增殖性DR(NPDR)和增殖性DR(PDR)。随着视网膜缺血和疾病进展加剧,DR可能由NPDR进展为PDR(图1),表现为视盘或视网膜新生血管(NVD&NVE)、玻璃体出血或视网膜纤维血管增殖和牵拉导致视网膜脱离,患者视力丧失的风险很大。DR长期以来被认为是微血管病变,但随着近年来基础研究和临床的快速发展,研究发现DR还表现为视网膜神经退行性病变和低中度炎症,涉及各种视网膜细胞、多种因素和途径。因此,如今DR被认为是由于慢性高血糖引起的视网膜神经血管单元(NVU)疾病或功能障碍。
随着DR严重程度升级,糖尿病黄斑水肿(DME)出现的频率增加,导致患者视力受损。在正常视网膜中,液体进出的维持受血-视网膜屏障(BRB)、Müller细胞和视网膜色素上皮(RPE)的正常功能调控。在DME的发病机制中,由于视网膜血管渗漏的增加以及Müller细胞和RPE细胞的引流功能障碍导致视网膜液体流入和流出不平衡,导致黄斑区液体积聚。根据Starling方程,渗漏的液体在视网膜内或视网膜下积聚,致使视网膜增厚和DME形成(图1)。在分子水平上,血管内皮生长因子(VEGF)和其他细胞因子参与了DME的发病机制,液体中细胞因子的基线水平可以作为DME抗VEGF治疗反应的预测指标。
图1. 一名31岁男性PDR及DME患者右眼眼底图像。A:超广角眼底照相显示多种微血管异常(黄色箭头所示),包括出血、硬性渗出、静脉串珠、视网膜内微血管异常(IRMA)、黄斑水肿、视盘新生血管(NVD)和视网膜其他部位新生血管(NVE)。B:OCTA显示右眼明显黄斑水肿。OCTA的B扫描显示混合型DME,表现为视网膜内液、囊样水肿(白色*)和视网膜下液(紫色#)积聚。在OCTA上黄斑颞上象限的浅表毛细血管丛中可见毛细血管丢失和无灌注区域{左上和左下(B)均用红色*表示}。
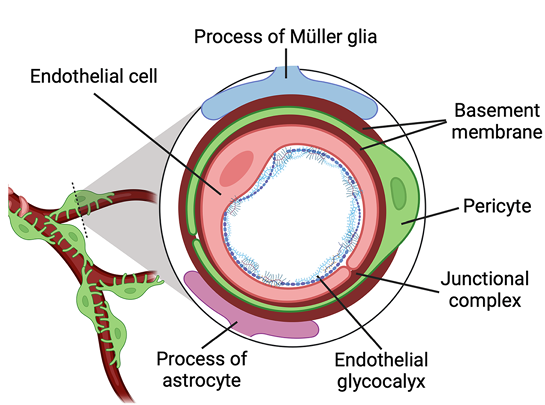
在正常的视网膜中,细胞(内皮细胞、周细胞、Müller细胞和星形胶质细胞)和非细胞(内皮糖萼和基底膜)组分构成了视网膜基本的血管单元(图2)。在这个血管单元中,细胞间互作、多种分子和细胞外基质(ECM)蛋白相互作用以及微血管稳定性都得到了很好的维持。DR可以通过不同的机制影响多种细胞和非细胞成分,导致微血管不稳定。微血管不稳定是导致DR和DME中iBRB破坏、血管渗漏和iNVU功能障碍的主要原因。
图2. 视网膜血管单元是iBRB维持视网膜微血管稳定性的基本单位,由细胞和非细胞组分构成。
iBRB和iNVU的细胞、分子组成以及iBRB的破坏
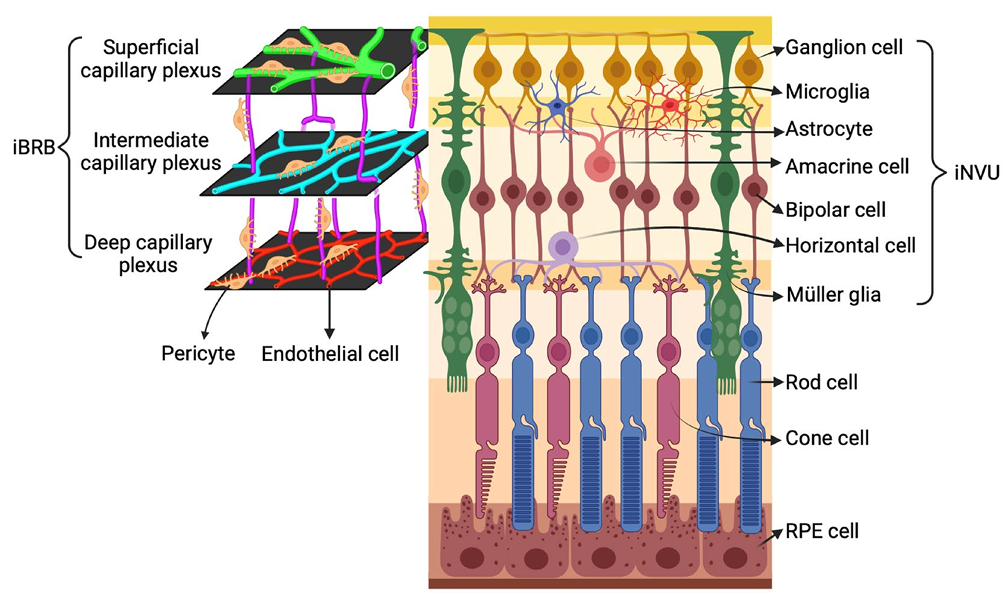
在正常视网膜中,视网膜微血管组成完整的iBRB以维持视网膜的正常功能,这为iNVU的组成、维持和稳定性提供了至关重要的支持。视网膜内皮细胞和周细胞,以及周围的Müller细胞和星形胶质细胞,共同形成了iBRB的细胞成分(图3)。神经胶质-血管串扰的正常功能和完整结构有助于维持iBRB和iNVU的正常功能。iBRB细胞成分的任何破坏最终都会导致视网膜微血管不稳定。
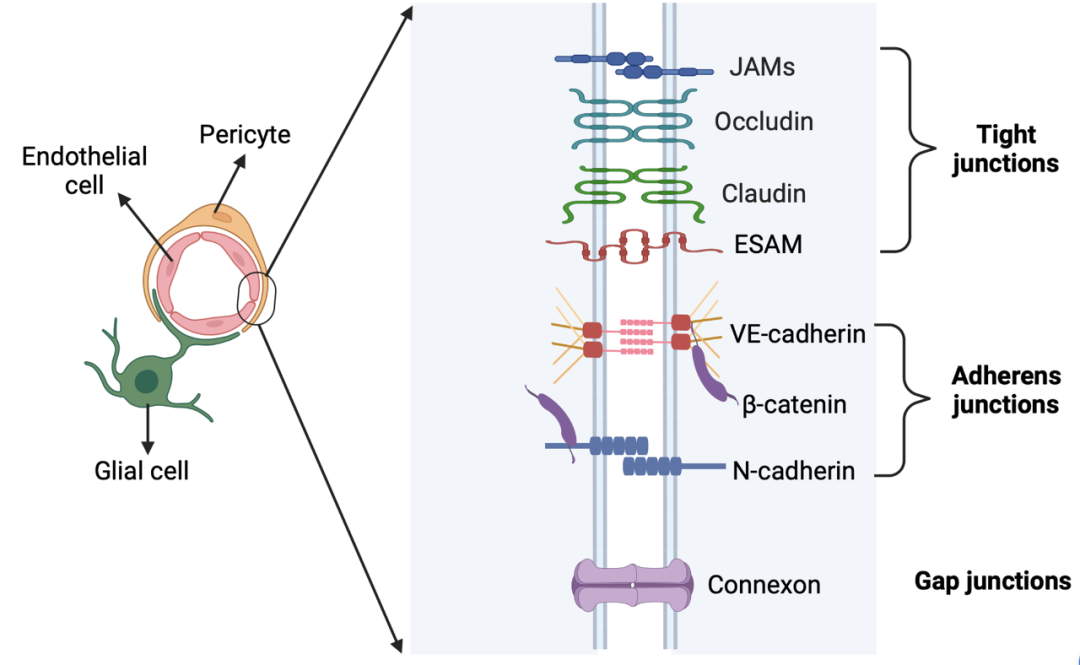
iBRB的完整性为iNVU的正常功能提供了保障。iNVU(图3)由视网膜血管细胞(内皮细胞和周细胞)、视网膜神经元(神经节细胞、无长突细胞、水平细胞和双极细胞)、神经胶质细胞(Müller细胞、星形胶质细胞和小胶质细胞)以及细胞外基质(ECM)蛋白组成。视网膜血管系统由小动脉、毛细血管和小静脉组成,管腔内侧由紧密连接的内皮细胞形成,内皮细胞排列在血管的管腔侧,直接面向血液,形成第一道细胞屏障。内皮细胞间完整的细胞间连接复合体(intercellular junctional complexes),包括紧密连接、粘附连接和缝隙连接,是维持iBRB结构和功能完整性的重要分子组分(图4)。内皮细胞被周细胞和神经胶质细胞(星形胶质细胞和Müller细胞)的突触紧密包裹,滋养内层视网膜神经元。不同的是:浅层毛细血管丛被Müller细胞和星形胶质细胞包裹,而深层毛细血管丛仅被Müller细胞包裹。在DR中,iNVU功能障碍表现为iBRB破坏、神经血管失调、视网膜细胞死亡、反应性胶质增生和小胶质细胞活化。iNVU的正常功能可以维持和协调视网膜中的神经血管耦合。
图3. 视网膜iBRB和iNVU的结构和细胞成分
图4. 视网膜血管内皮细胞间连接复合体
DR的主要特征是微血管改变,包括基底膜增厚、内皮细胞之间紧密连接的破坏或缺失、周细胞和内皮细胞的丢失或脱落、无细胞性毛细血管形成、血管通透性增加、毛细血管闭塞、微动脉瘤、IRMA等。糖尿病影响iBRB,导致神经血管耦合失调,iNVU功能障碍。在DR中,iBRB功能改变可作为微血管不稳定的一种表现,其特征是血管通透性增加以及视网膜血流的失调。微血管稳定性的降低,最终导致血管细胞丢失、通透性增加、炎症,甚至新生血管,导致视网膜血管满足神经元代谢需求的能力降低,进一步影响iNVU的功能。因此,iBRB的破坏和iNVU的功能障碍可导致DR的微血管病变和神经变性,这可能被视为治疗靶点。作为iBRB和iNVU的基本单元,视网膜血管单元(图2)包含细胞外基质,包括内皮糖萼和血管基底膜,可维持iBRB和iNVU的稳态和正常功能。
基质和细胞间互作在维持微血管稳定中发挥作用
基底膜增厚促进糖尿病微血管病理发展,这在大多数组织中均有体现,例如视网膜、肾脏、肌肉和皮肤。越来越多的数据表明,基底膜增厚会影响细胞联系、调节细胞代谢和物质交换,从而影响DR中细胞存活和新生血管形成。此外,高糖会使基底膜变硬,改变血管弹性,从而损害周细胞对视网膜血流的调节能力,进一步促进内皮细胞的活化,内皮细胞通过增加细胞间黏附分子-1(ICAM-1)和促进白细胞粘附来介导炎症。
许多视网膜细胞构成iBRB和iNVU,这些细胞之间的相互作用对iBRB和iNVU的正常功能起着关键作用。iNVU内的复杂相互作用要求每个细胞以协调一致的方式运作,以确保iBRB对视网膜稳态的调控(图3)。复杂的细胞间互作包括直接(即内皮细胞与内皮细胞、胶质细胞与胶质细胞、周细胞与内皮细胞和细胞-基质相互作用)和间接(即Müller细胞与内皮细胞、小胶质细胞与内皮细胞)相互作用,详见原文说明。
DR中细胞因子和信号通路的改变以及复杂的分子网络
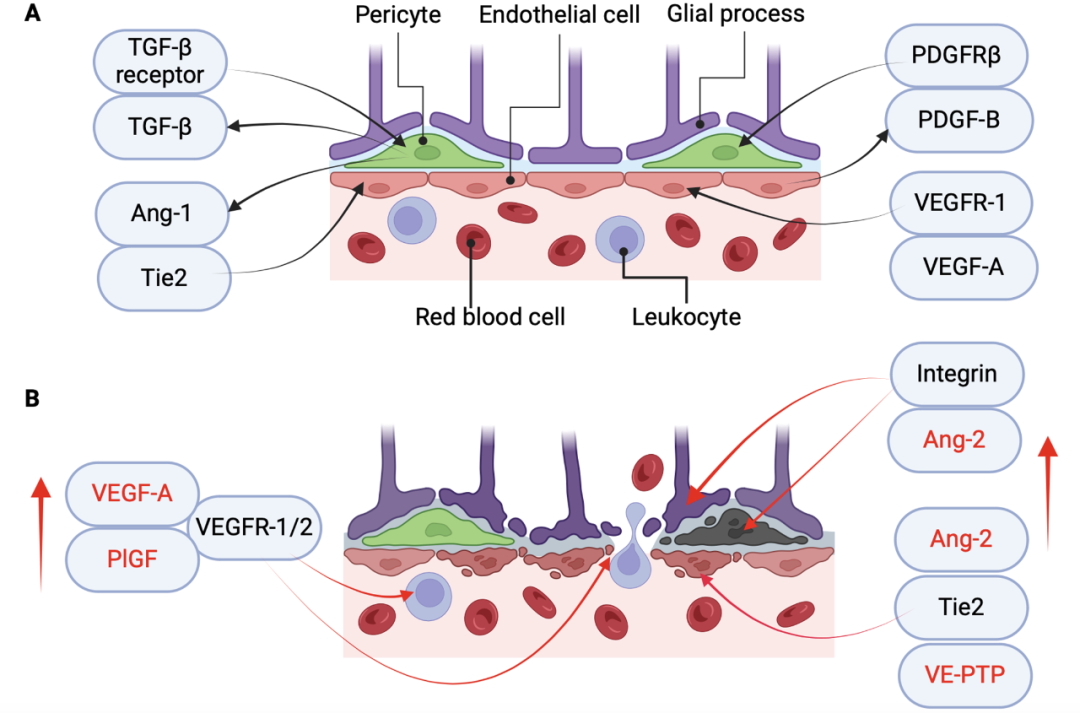
在DR发病过程中,包括缺氧、异常生长因子、细胞因子、炎性细胞因子和活性氧(ROS)增加等诸多因素都参与了微血管不稳定。缺氧可稳定低氧诱导因子(HIF)-1α,其与HIF-1β形成二聚体并转移到细胞核,刺激缺氧调节的基因表达,如VEGF、PIGF、血管生成素-2(Ang-2)、血管内皮蛋白酪氨酸磷酸酶(VE-PTP)等。这些因素相互关联,共同作用,导致微血管不稳定(图5)。在这些因素中,VEGF及其受体是血管渗漏和视网膜新生血管形成的主要刺激因素,而Ang-2和VE-PTP通过抑制Tie2使内皮细胞对VEGF更敏感,共同导致DR和DME的发病。参与微血管不稳定的几种生长因子和激活途径详见原文。
图5. 视网膜血管单元中内皮细胞和周细胞在正常和疾病状态下的分子相互作用
研究结论与展望
iBRB的破坏导致iNVU血管通透性增加、视网膜水肿和神经视网膜损伤,进而导致DR患者视力丧失。其中,微血管不稳定是导致iBRB破坏的主要原因。微血管不稳定是由升高的生长因子和细胞因子、持续炎症以及高血糖、缺氧或其他损伤引起的周细胞和/或内皮细胞的脱落/丢失/死亡等组合效应所引起的。随后,液体经过细胞旁途径和跨细胞途径渗漏增加。iBRB非细胞组分(内皮糖萼和ECM)的功能和结构变化进一步促进和加重iBRB的破坏,导致iNVU的高渗透性、黄斑水肿,甚至神经视网膜损伤和功能障碍。
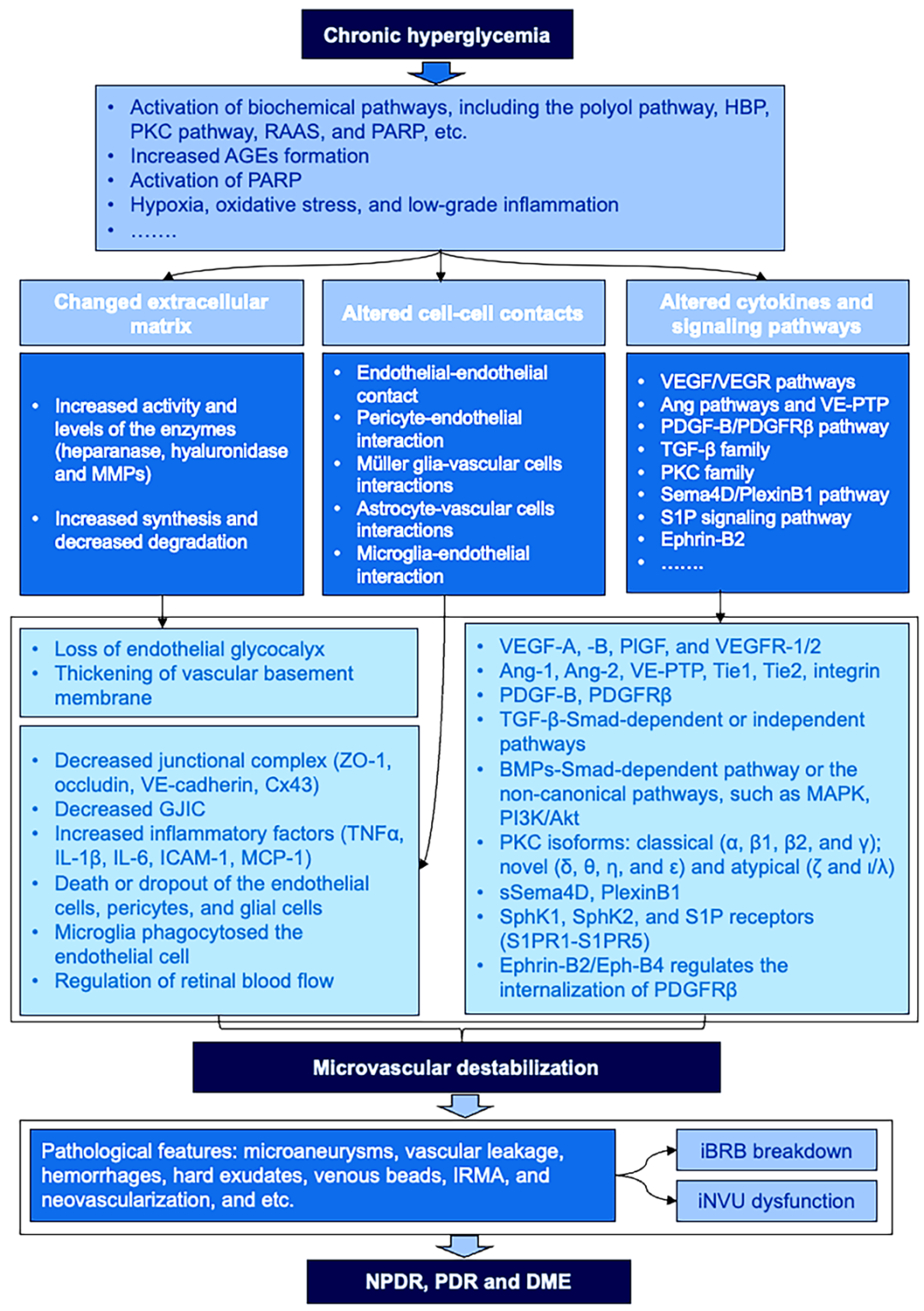
iBRB的破坏和iNVU的功能障碍主要是由于视网膜微血管不稳定,涉及DR中复杂的细胞和分子过程(图6)。近年来,DR微血管不稳定研究进展迅速,靶向关键分子或特定的iBRB细胞将为合理设计旨在稳定视网膜微血管的药物提供支持,进而恢复iBRB和iNVU的功能和结构,最终造福DR和DME患者。
图6. 视网膜微血管不稳定涉及多种因素,最终导致DR及DME
综述原文:
Sheng et al. Cell & Bioscience
https://doi.org/10.1186/s13578-024-01269-7
作者介绍
通讯作者:张敬法教授
香港中文大学(深圳)国际眼科研究所协同所长、兼职教授、博导;希玛眼科(深圳)眼底病科主任、眼基础研究主任;希玛眼科(香港)眼科学研究总监。担任第40届亚太眼科学会(APAO)大会视网膜(医学)项目秘书、中国医师协会眼科医师分会第五届基础研究与临床转化副主任委员(兼秘书)、中国老年医学学会眼科分会青年委员会副主任委员、上海市生物医药行业协会精准医疗专业委员会常委、上海市衰老与退行性疾病学会老年医学转化分会常委、上海市医学会眼科专科分会视觉研究学组组长等。原上海市眼科研究所副所长,研究员,副主任医师,博士研究生导师。临床及科研方向为眼底病发病机制及治疗,聚焦糖尿病视网膜病变和年龄相关性黄斑变性。
免责声明:上述内容仅代表发帖人个人观点,不构成本平台的任何投资建议。