以色列 一家医药公司 Gamida Cell IPO简介
摘要: 以色列 一家医药公司 Gamida Cell向美国证券交易委员会的IPO文件, 预计以6900万美元公开发行股票;股票代码: GMDA, IPO承销商: BMO Capital Markets和RBC Capital Markets, 对于想知道如何购买 Gamida Cell 股票的朋友 可以提前研究了, IPO时间为: 2018-10-26。 $Bausch Health Companies Inc(BHC)$ $普罗基尼克斯制药(PGNX)$ 原文
概要
Gamida Cell的主要产品是NiCord,这是一种III期NAM扩增的脐带血细胞疗法。该公司认为,它有可能成为需要造血干细胞移植的患者的通用治疗干细胞移植物。III期试验招募患有多种恶性血液病的患者,包括高风险白血病,如急性髓性白血病(AML),急性淋巴细胞白血病(ALL),慢性粒细胞白血病(CML),骨髓增生异常综合征(MDS)和淋巴瘤。Gamida Cell表示,它预计将在2020年上半年进行第三阶段试验的最佳数据。
在I / II期试验中,Gamida Cell表示,移植NiCord的患者实现了快速植入和免疫重建,这是临床获益的关键指标。作为I / II期试验的结果,美国食品和药物管理局(FDA) 于7月向NiCord 授予Orphan药物指定用于造血干细胞移植(HSCT)。Gamida Cell表示,NiCord之前曾被授予Orphan Drug Designation作为治疗几种血液系统恶性肿瘤的药物。该公司表示,NiCord还获得了欧洲药品管理局的同名称号。
在其提交给美国证券交易委员会的文件中,Gamida Cell表示除了血液系统恶性肿瘤外,该公司还在开发NiCord作为骨髓衰竭疾病的治疗方法。美国国立卫生研究院(NIH)正在对患有严重再生障碍性贫血(一种罕见的危及生命的血液疾病)的患者进行I / II期试验,对NiCord进行评估。Gamida Cell表示,该试验的初步数据预计在2019年。
除了NiCord,Gamida Cell也在开发NAM-NK作为癌症治疗。NAM技术利用具有抗肿瘤特性的天然杀伤细胞的能量。NAM-NK“通过增加细胞毒性以及在培养条件下扩增的NK细胞的体内保留和增殖来解决NK细胞治疗潜力的关键限制,”该公司表示。NAM-NK目前正在进行研究者资助的1期试验,用于治疗难治性非霍奇金淋巴瘤和多发性骨髓瘤。
在过去的几个月里,Gamida Cell一直在加强其领导团队的几项重要任命。最近,该公司任命Cytokinetics公司总裁兼首席执行官罗伯特·布鲁姆为该公司董事会主席。Gamida Cell的首席执行官兼前任董事长朱利安•亚当斯(Julian Adams)将留在公司的董事会。其他任命包括Jaren Madden担任投资者关系主管,Tzvi Palash担任首席运营官,John Schick担任市场准入负责人。今年早些时候,该公司还任命了一名新的首席商务官,营销负责人,并任命Shai Lankry为其首席财务官。
公司简介
Gamida Cell是一家总部设在以色列耶路撒冷的以色列公司,成立于1998年。Gamida Cell的主要执行办公室位于以色列耶路撒冷91340 Givaat Shaul的Nahum Heftsadie St.,Gamida Cell的美国子公司的执行总部位于马萨诸塞州的波士顿。Gamida Cell的电话号码是+972(2)659-5666。Gamida Cell的网站地址是www.gamida-cell.com。Gamida Cell网站上包含的信息以及通过Gamida Cell的网站提供的信息仅为非活动文本参考。
Gamida Cell是一家临床阶段的生物制药公司,利用Gamida Cell的专有技术开发旨在治疗癌症和罕见的严重血液疾病的细胞疗法。虽然细胞疗法具有解决各种疾病的潜力,但它们受到供体细胞的可用性,供体与患者匹配以及当扩增细胞以达到治疗剂量时供体细胞功能性下降的限制。Gamida Cell利用基于烟酰胺(或NAM)的细胞扩增技术开发了一系列产品,旨在解决细胞疗法的局限性。Gamida Cell的专有技术旨在促进供体细胞的增殖,同时保持细胞的功能性治疗特性,如果获得批准,将为患者提供治疗选择。
Gamida Cell最先进的候选产品NiCord是一种NAM扩增的脐带血细胞疗法,有望成为需要造血干细胞移植或HSCT的患者的通用治疗性干细胞移植物。该公司目前正在为120名患有各种血液系统恶性肿瘤的患者进行关键的3期临床试验,其中包括高风险白血病,如急性髓性白血病,或AML,急性淋巴细胞白血病或ALL,慢性粒细胞白血病或CML,骨髓增生异常综合征,或MDS和淋巴瘤。Gamida Cell预计将在2020年上半年报告该试验的最佳数据。在Gamida Cell的1/2期临床试验中,移植了NiCord的患者实现了快速植入和免疫重建,这是临床获益的关键指标。根据Gamida Cell的1/2期临床试验结果,Gamida Cell从美国食品药品管理局或FDA获得了美国NiCord的突破性治疗指定。此外,Gamida Cell还获得了FDA和欧洲药品管理局的孤儿药指定。
除血液系统恶性肿瘤外,Gamida Cell正在寻求开发用于治疗骨髓衰竭疾病的NiCord。NiCord目前正在由美国国立卫生研究院(National Institutes of Health)赞助的1/2期临床试验中进行评估,该试验用于患有严重再生障碍性贫血的患者,这是一种罕见的危及生命的血液疾病。本研究旨在评估NiCord移植的安全性和有效性,以克服与常规脐带血相关的严重再生障碍性贫血的移植排斥反应的高发生率。Gamida Cell期望在2019年报告Gamida Cell的1/2期临床试验的初步数据。
除了NiCord,Gamida Cell利用Gamida Cell的NAM技术开发另一种候选产品NAM-NK,用于扩增的自然杀伤细胞或NK细胞的先天免疫治疗,与标准治疗抗体结合使用。NK细胞具有有效的抗肿瘤特性,并且具有优于其他不需要遗传匹配的肿瘤细胞疗法的优势,当与某些抗体组合时,可能使NK细胞成为基于供体的通用疗法。NAM-NK通过增加培养条件下扩增的NK细胞的细胞毒性和体内保留和增殖来解决NK细胞治疗潜力的关键限制。NAM-NK目前正在进行研究者资助的1期试验,用于治疗难治性非霍奇金淋巴瘤和多发性骨髓瘤或MM。
下图总结了Gamida Cell当前候选产品系列的关键信息:
Aplastic贫血研究新药(IND)申请目前已在FDA以品牌名称CordIn提交,该名称与NiCord一样是研究性开发候选人。
NiCord治疗血液系统恶性肿瘤
同种异体HSCT的局限性
细胞疗法涉及递送人细胞以替换或修复受损组织或细胞以治疗多种癌症和其他疾病。HSCT,通常称为骨髓移植,是最常用的细胞疗法,用于治疗各种血液系统恶性肿瘤和其他严重疾病。一个人的全血和骨髓可以从同种异体或非自身供体的干细胞种子群体中重建,该血液形成和免疫系统形成细胞都没有癌症,并有效地实现了它们功能。在美国进行的大约90%的HSCT程序用于恶性血液病患者。在美国,欧洲和日本,每年大约有30,000名患者接受同种异体HSCT,其中8名患者,500人在美国。从2006年到2016年,这些程序的数量在美国每年增加5%。到2021年,公司预计大约11,000名患有恶性血液病的人将成为HSCT的候选人,而公司进一步预测NiCord,如果批准,将用于治疗约30%的这些患者。
尽管HSCT具有治愈潜力,但据估计,多达40%的符合条件的患者由于各种原因未能获得HSCT,包括找到匹配的供体。供体细胞的最佳来源是兄弟姐妹,它是匹配的相关供体或MRD,但在美国与兄弟姐妹匹配的可能性仅为25%至30%。大多数患者依赖于供体细胞的替代来源,包括匹配的无关供体,或MUD,半相合或“半匹配”供体和脐带血。尽管供体细胞具有各种潜在来源,但HSCT受到许多重大限制,包括:(i)延迟寻找合适的匹配,在此期间疾病进展可能使患者不适合移植; (ii)供体细胞数量不足或延迟植入,让患者无免疫系统功能,导致移植后可能危及生命的免疫缺陷; (iii)供体细胞与患者自身细胞之间缺乏长期相容性,导致可能致命的移植物抗宿主病或GvHD。
对于需要HSCT并且没有MRD来源的患者,脐带血有望作为干细胞的现成来源。当使用源自脐带血的干细胞时,更容易找到匹配,因为使用脐带血成功移植不需要完全匹配。这扩大了潜在捐助者的范围,缩短了寻找合适匹配的过程。然而,平均而言,典型的脐带血移植物含有大约干细胞和祖细胞数量的十分之一
与来自成人骨髓或外周献血者的干细胞移植物相比。这种较低数量的细胞可延迟供体细胞的植入和免疫系统的重建。反过来,这又增加了医院的时间和患者可能感染危及生命的感染的可能性。
NiCord作为异基因HSCT的通用干细胞移植物
Gamida Cell的主要候选产品NiCord旨在解决HSCT和脐带血作为供体细胞来源的局限性。NiCord由脐带血组成,使用Gamida Cell专有的基于NAM的细胞扩增技术制造,旨在提高HSCT的植入效率,并实现快速植入和免疫系统重建。这降低了移植后感染和其他并发症的风险。此外,脐带血中的供体T细胞是幼稚的,这意味着它们尚未成熟并且可能更容易适应接受者。这导致更大的免疫相容性,或供体细胞与受体细胞的匹配,降低GvHD的频率和严重性。鉴于这些优势,NiCord如果获得批准,可以作为一种普遍的,易于获得的,
Gamida Cell目前正在招募患者进行国际,多中心,随机,关键的3期临床试验,对120名血液系统恶性肿瘤,AML,ALL,CML,MDS和淋巴瘤患者进行研究。Gamida Cell预计将在2020年上半年报告该试验的最佳数据。在Gamida Cell赞助的1/2期临床试验中,Gamida Cell招募了36名血液系统恶性肿瘤患者,这些患者没有合适的匹配供体。为了比较,Gamida Cell从国际血液和骨髓移植研究中心(CIBMTR)收集的数据中确定了146名患者作为历史对照。基于中性粒细胞的恢复,中性粒细胞植入的主要终点得到满足,中性粒细胞是抗感染白细胞。中性粒细胞植入定义为实现至少0.5×10 9的最小嗜中性粒细胞计数不同日期连续三次测量每升。在NiCord治疗的患者中移植后中位恢复时间为11.5天,而历史对照组为21天。一项关键的次要终点,血小板植入,在NiCord治疗的患者中也达到了34天的中位恢复时间,而历史对照组为46天。血小板是正常血液凝固所必需的,低血小板计数与危及生命的出血有关。血小板植入定义为实现至少20×10 9的血小板计数在不同日期连续三次测量每升,在前七天没有血小板输注。与使用标准脐带血治疗的类似患者相比,有效植入和强大的免疫重建可能有助于观察到移植后患者住院天数减少20天。根据第1/2阶段试验的结果,Gamida Cell获得了FDA的突破性治疗指定。
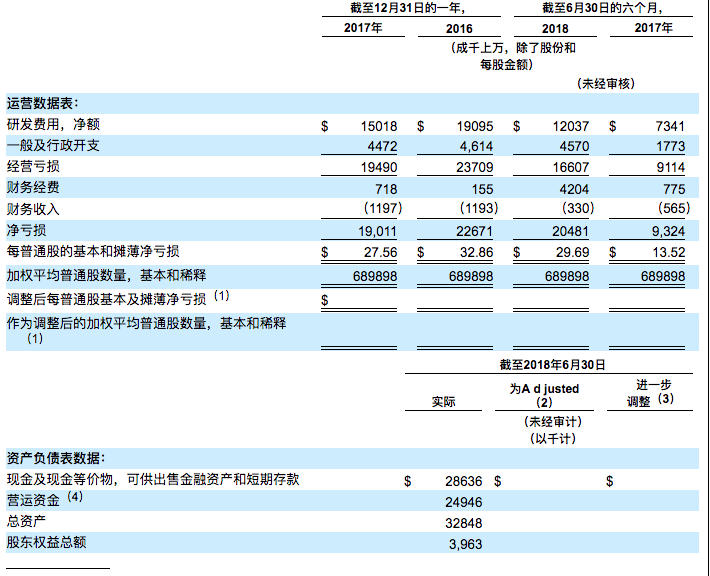
财务报告
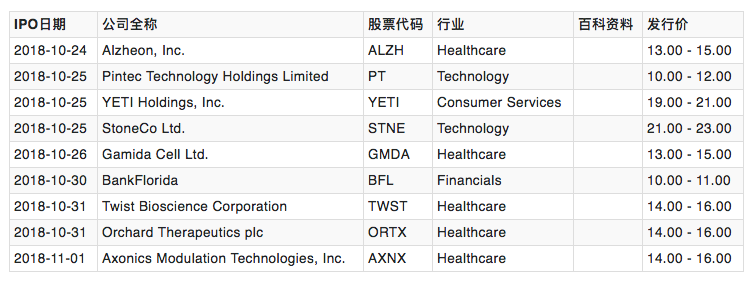
最近上市的一些公司列表
相关信息
- [如何购买 Gamida Cell 股票]
- Gamida Cel 股票代码: $(GMDA)$
- Gamida Cel SEC 文件
- 更多内容 请关注我的微信公众号: 美股指南
免责声明:上述内容仅代表发帖人个人观点,不构成本平台的任何投资建议。
- NEXTTOME·2018-10-26感谢分享了~点赞举报