公司介绍
IceCure Medical Ltd (冰疗医疗有限公司)为女性健康和肿瘤学市场开发和销售微创冷冻消融疗法,专注于基于液氮或 LN2的冷冻消融系统和技术的研究、开发和营销,用于治疗肿瘤。冷冻消融是通过冷冻患者体内的良性和恶性肿瘤来消融(破坏)这些肿瘤的过程。我们专有的冷冻消融技术是手术干预的微创替代方案,适用于肿瘤,包括在乳房、肺、肾、骨骼和其他适应症中发现的肿瘤。
该公司成立于 2006年,总部位于以色列凯撒利亚。它通过以下地理分区运作:以色列、日本、美国、中国、西班牙、泰国和其他国家。该公司成立于2006年,总部设在以色列西泽利亚。
产品介绍
该公司提供 ProSense系统,这是一种用于乳腺肿瘤的冷冻消融解决方案。(如图所示)
公司除了现有的主导产品 ProSense系统,一个单探针系统,公司还开发了一个额外的多探针系统,预计能够同时冷冻多个肿瘤或更大的肿瘤,公司将其称为 MultiSense系统。而这些系统需要获得针对特定适应症的现有和下一代产品的监管批准。截至 2021年 8月,公司的系统已获得广泛的监管批准,用于治疗肺部、肾脏、骨骼和其他适应症的肿瘤。在美国,公司的产品被批准为称为“IceCure系列”的“单一系列”,其中包括 IceSense3、ProSense和 MultiSense(尚未商业化)冷冻消融系统。尽管公司现有的“IceCure系列”系统已获得美国食品和药物管理局 (FDA)的监管批准,可在美国进行商业化,但公司尚未获得此类系统治疗恶性乳腺肿瘤的监管批准。需要获得 FDA的单独批准。 FDA根据医疗器械的风险水平和确保器械安全性和有效性所需的控制类型,将医疗器械分为三类(I类、II类或 III类)之一。课程分配是确定在美国销售产品之前所需的上市前提交或申请类型(如果有)的一个因素。如果 FDA不批准 510(k)监管途径,公司将要求“IceCure系列”系统接受 De Novo分类。如果公司的“IceCure系列”系统需要从头分类,公司将被要求接受 FDA施加的特殊控制,主要是生产过程和上市后监控。如果 FDA不批准 De Novo分类作为监管途径,FDA将只接受上市前批准或 PMA,在这种情况下,公司预计上市批准的时间会更长,公司与 PMA相关的成本将是与 510(k)或 De Novo批准相比更高。这边我们简单的理解下就是,虽然IceCure系列已经得到了FDA批准,可以商业化,但是公司对于治疗恶性乳腺肿瘤的资质还没得到批准。
行业表现
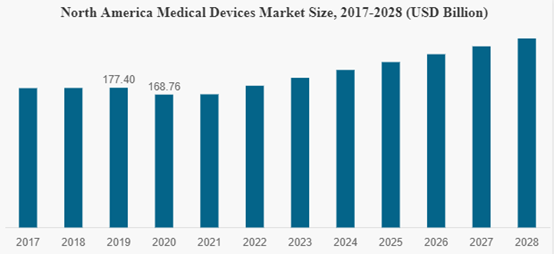
2020年全球医疗器械市场规模为4322.3亿美元。受到新冠疫情的影响,大流行期间对所有地区采用医疗器械率产生了负面影响。根据分析,2020年全球市场下降了3.7%。预计该市场将从2021年的4553.4亿美元增长到2028年的6579.8亿美元,2021-2028年期间的复合年增长率为5.4%
医疗技术公司在研发方面的投资增加以及监管部门为其批准提供的有利场景预计将在未来推动医疗器械行业的发展。例如,根据美国FDA数据显示,在2019年-2020年期间,大约有59台设备获得FDA批准。
财务报告
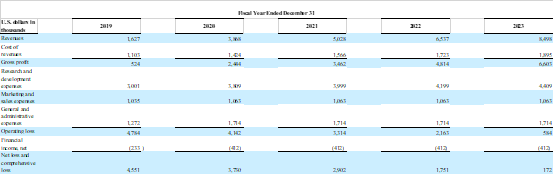
- 公司收入主要包括销售 ProSense系统及其一次性用品和相关服务; 将公司的产品在日本和新加坡的独家经销权授予 Terumo Corporation的收入,其中还包括提供技术、监管和临床材料以及获得监管批准的支持。
- 公司2019年、2020年的收入为$162万、$386万,同比增长137%。
- 公司目前处于亏损状态,不过亏损额度有所下降,从2019年的$455万到2020年的$373万。主要因为收入增长,收益成本降低。
预期成长
目前公司还处于初期阶段,目前收入基本靠单一的产品销售,虽然有其它产品处于研发或者是正在申请批准阶段,但是这需要等待比较长的一段时间,快则一年能获得审批,慢则需要整改等需要3年时间。但是随着公司的扩张,其销售能力肯定会提高,成本可能会进一步压低。所以在这期间,公司预计能在3年内实现盈利。
投资有风险,入市需谨慎,以上观点只是个人见解,各位看官需按照自己需求判断。
@小虎活动@爱发红包的虎妞 @小虎AV@Tony特别帅


精彩评论