基本概念
1、精准医学:
- 精准医学是利用基因测序技术、基因编辑技术,综合患者生活环境和临床数据,
- 实现精准的疾病分类及诊断,制定具有个性化的疾病预防和治疗方案。
2、Pipeline:
- 企业制药研发管线,一系列新药上市前列临床试验和审批流程。
3、FDA批准上市前后需要经过哪些临床阶段:
I期临床试验:
- 进行初步的临床药理学及人体安全性评价试验,
- 观察人体对于新药的耐受程度和药代动力学,
- 为制定给药方案提供依据医|学教育网搜集整理。
Ⅱ期临床试验:
- 是初步评价药物对目标适应证患者的治疗作用和安全性,
- 也包括为Ⅲ期临床试验研究设计和给药剂量方案的确定提供依据。
III期临床试验:
- 增加样本量并根据试验目的的调整选择受试者标准,
- 适当扩大特殊受试人群,用更为丰富的观察项目或指标等措施,进一步考察不同对象所需剂量及依从性。
- Ⅲ期临床试验的条件应尽可能接近该药的正常使用条件,
- 试验药要经中国药品生物制品检定所检定合格,供药时,标明药物系专供临床试验用。
Ⅳ期临床试验:
- 是新药上市后由申请人自主进行的应用研究阶段。
- 其目的是考察在广泛使用条件下药物的疗效和不良反应;
- 评价在普通或者特殊人群中使用的利益与风险关系;改进给药剂量等。
- 弥补上市前临床试验缺乏的资料和信息,为临床合理用药提供依据。
4、FDA加快新药上市的4种审批方式:
快速通道:
- 该审评方式是用来促进和加速用于治疗严重疾病且有可能解决无法满足目前医疗需求药物的审评方式,
- 能够加速新药的研发和审评。
突破性疗法通道
- 是2012 年9 月FDA 首创的一种新药审评方式。
- 需满足两个条件:
- 药物适应症是严重或致死性疾病,
- 以及有证据显示目标药物在某一重要临床终点上明显优于现有药物。
- 突破性疗法通道的认定比快速通道更加严格,享有快速通道的所有优势,能得到FDA更加密切的指导。
在接下来的文章中,将经常看到突破性疗法通道的授予,这个通道基本上就是FDA为精准医学专门设立的通道。
优先审评
- 适用于目标药物有优于现有治疗手段的可能。
加速审批
- 旨在使患者早日得到重要的新药治疗。
概要:
1、市场核心驱动力:技术突破和重要临床进展。
2、行业处于早期阶段,大部分公司处在VC阶段,上市企业也大多处于亏损状态,医药巨头在积极布局。
3、投资风险高,建议早期阶段仅考虑投资诺华、葛兰素史克这种布局该行业的医药巨头。
行业研究
1精准医学前沿技术及应用
1.1基因编辑技术
基因编辑技术是指对目标基因进行精确操作,实现基因的定点插入、删除,以达到启动或关闭目标基因的目的。
基因编辑技术是细胞免疫技术和基因治疗的基础。
1.2细胞免疫治疗技术
免疫系统如何杀死肿瘤
免疫系统可以识别并清除“非己”物质的,这个过程叫免疫应答,这是我们体内天然的自我保护机制。
CAR-T技术和TCR-T技术,其根本的方法,就是通过基因编辑技术,让T细胞表达可以有效识别体内癌细胞的特异性抗体,从而达到杀死这些癌细胞的目的。
区别就在于CAR-T是人工合成整个T细胞受体的三块结构,而TCR-T是指改变受体的识别区的CDRs。
这些CDRs就是在这个领域常说的靶点。
可以看到CDRs无论在CAR-T还是TCR-T技术中,都起着至关重要的作用,也是免疫细胞疗法针对不同癌症研究的重中之重。
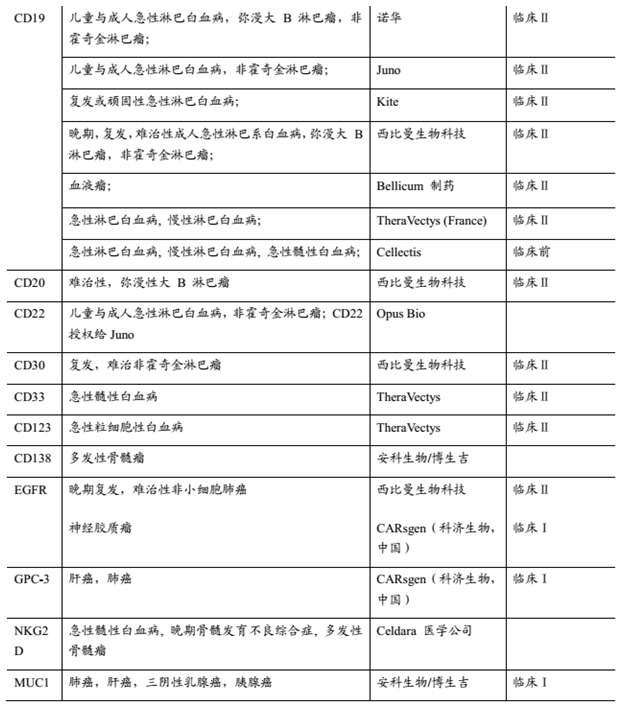
下面的表格是精准医学公司针对不同癌症类型对应研究的不同靶点。
可以看到,诺华、Juno、Kite主要研究的靶点是CD19,这个靶点在血液癌症中扮演重要的角色。
而在肺癌和肝癌中,EFGR和GPC-3靶点是主要的研究对象。
总结:CAR-T和TCR-T是细胞免疫治疗中两个最重要的技术,这两种技术目前都取得了一定的成就,它们是承载着人类攻克癌症的全部希望的。
1.3基因治疗技术
基因治疗是通过基因编辑技术,将新的基因插入到病人的细胞中,代替丢失或发生故障的基因,从而达到治疗病症的效果。
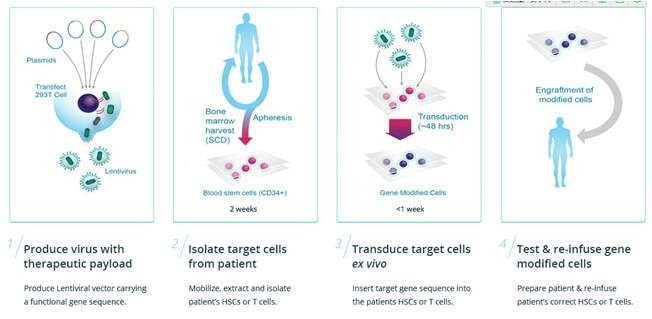
首先,从病人体内抽取血液或者骨髓,从中提取出未成熟的细胞,将新的基因通过基因编辑技术插入细胞内,
再将这些细胞注入到病人血液中,这些细胞在病人体内通过血液循环进入到骨髓时,会变成熟,并快速繁殖,
最终全部取代有缺陷的细胞。
2精准医学行业的主要玩家
2.1基因编辑公司
基因测序和基因编辑是细胞免疫治疗和基因治疗的基础,所以基因编辑类公司属于精准医学这个行业的上游企业,他们广泛的与其他公司合作,为临床实验提供基因编辑服务。
Editas Medicine公司$(EDIT)$
2013年由麻省理工华裔教授张锋和Jennifer Doudna二人成立,他们是CRISPR技术的最早发明人,
尤其是张峰,可以说是这个技术的先驱。精通CRISPR/Cas9技术和TALEN技术。
但由于在CRISPR的专利申请问题上存在的矛盾,Jennifer Doudna在2014年左右离开了EDIT,并把她的那部分专利卖给了Intellia Therapeutics。
今年2月份于Nasdaq上市。
今年5月份,EDIT与Cystic Fibrosis Foundation Therapeutics(CFFT)宣布了一项为期3年,价值500万美元的合作,基于CRISPR技术的囊肿性纤维化的开发。
CRISPR Therapeutics公司
CRISPR Therapeutics是第二家主攻CRISPR技术的公司,由Emmamuelle Charpentier创立。
关于CRISPR的发明过程,张峰肯定是先驱性人物,
但是让科学界真正意识到CRISPR的价值的,是Jennifer Doudna和Emmamuelle Charpentier分别发表的两篇学术论文,
所以CRISPR的专利申请一直比较复杂,Emmamuelle Charpentier也算是共同发明人之一。
2015年10月,Vertex与CRISPR Therapeutics展开合作,签约四年开发囊肿性肺纤维化和镰刀型贫血症的药物,
如果都能上市,Vertex将支付CRISPR Therapeutics26亿美元。
2015年12月,CRISPR Therapeutics与拜耳合作开发血友病、失明及先天性心脏病等药物,计划5年内注资5亿美元。
Intellia Therapeutics$(NTLA)$
在得到了Jennifer Doudna的授权之后,Intellia Therapeutics于2014年成立。
与CAR-T技术处于领先地位的诺华展开了长达5年的合作计划,致力于CRISPR技术在CAR-T中的应用。
2015年与Regeneron达成为期6年的开发协议,开发10种药物。
今年5月在Nasdaq上市。
2.2.细胞免疫治疗公司
Novartis$(NVS)$
诺华是国际制药巨头中最早进入细胞免疫治疗的公司,也是目前临床数据最领先的企业。
2012年,诺华与CAR-T技术研究最先进的宾夕法尼亚大学合作,开发CD19靶点的CAR-T技术,又在宾夕法尼亚大学建立了全球首个综合性CAR-T细胞疗法开发中心。
正是在诺华与宾大合作这一年,June团队用CAR-T技术,成功消灭的Emily Whitehead的全部癌细胞,治愈了她的急性淋巴细胞白血病(ALL),
至今Emily已经四年Cancer-free。
2014年7月,诺华基于治好Emily Whithead急性林白细胞白血病的CAR-T技术开发的药物CTL019获FDA突破性疗法认定,药物研发完毕后享受一切FDA审批的绿色通道。
目前,诺华的这款细胞产品已经到了商业级别,将支持产品的全球临床试验。预计这款产品今年年内能获批。
Juno Therapeutics$(JUNO)$
JUNO是由Fred Hutch癌症中心、Memorial Sloan Kettering癌症中心和西雅图儿童中心三家美国赫赫有名的医学机构强强联合,组建的医学研究中心。
2014年登陆Nasdaq。Juno目前处于临床试验中的项目有10个,涵盖6种产品,4个靶点,及CAR-T和TCR-T两种技术。
其中JCAR015获得了FDA突破性疗法认定。
JCAR015也是用于治疗成人急性淋巴细胞白血病(ALL)的,目前临床2期,完全缓解率达到89%。
完全缓解的意思就是癌细胞完全消除。这意味着有89%的病人的白细胞完全消除。
而用于治疗复发/难治性CD19白血病的JCAR017,完全缓释率也达到了85%。
但就在前天,7月8号,JCAR015被FDA叫停。有两个病人因神经中毒死亡。
Juno这次临床二期被叫停的药物JCAR015,赶上了白血病的一种不常见的情况,就是中枢神经系统白血病,
白血病细胞侵犯蛛网膜,进入到了中枢神经系统,而CAR-T追踪到了中枢神经里,并在那大量杀死癌细胞,导致了这起中枢神经中毒死亡事件。
下表是Juno目前的Pipeline:
Kite Pharma$(KITE)$
也是同时兼顾CAR-T技术和TCR-T技术的公司。
其中CAR-T技术的KTE-C19产品获得FDA突破性疗法通道,这款产品用来治疗儿童非霍奇金淋巴瘤(NHL),这是一种常见的恶性肿瘤。
在所有恶性肿瘤里排名前10。目前临床2期的结果是完全缓解率57%;总体应答率71%。
值得注意的是,KITE在TCR技术用于固体肿瘤的研究中,也有6种产品进入临床试验中。
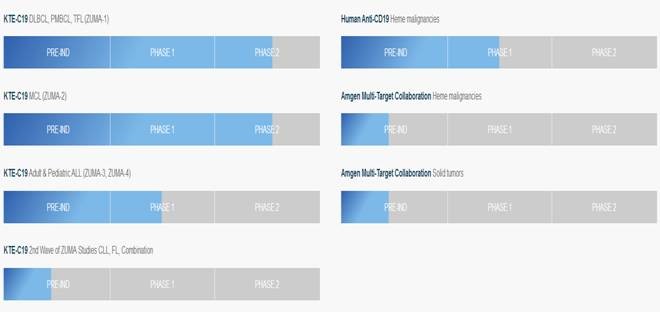
下面分别是KITE的CAR技术和TCR技术的Pipeline:
CAR
TCR
Cellectis公司
异体CAR-T第一家。
其他公司的CAR-T都来自于病人本身,
但Cellectis的T细胞来自健康的捐献者,他们通过TALEN基因编辑技术,敲出了T细胞上原有的TCR,消除组织相容性问题。
这一技术大大的降低了CAR-T的应用成本,因为不再局限于单个个体细胞的基因编辑,而是扩展到能生产出一个人群都能的到适用的CAR-T。
2015年底,Cellectis开发的UCART19在一个11个月患有急性淋巴细胞白血病的婴儿Layla Richards身上进行成功的临床治疗,
Layla被完全治愈,同时也吹响了CAR-T技术和基因编辑技术产业化的号角。
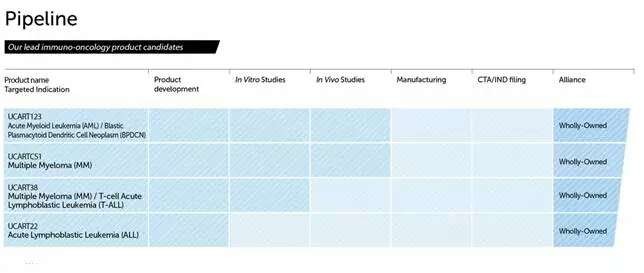
Cellectis的 Pipeline
Bellicum $(BLCM)$
这个公司是CAR-T 安全开关的创造者,核心技术是CID(化学诱导二聚体)。
原理是把CAR中的识别域和激活域分开,移到分离的分子开关上,再通过小分子药物rimiducid控制T细胞的诱导凋亡和激活增殖。
Adaptimmune$(ADAP)$
专注于TCR-T技术。
其中,以NY-ESO作为靶向的T细胞疗法被FDA授予突破性疗法资格。
这种疗法适用于肿瘤有表达NY-ESO抗原的手术不可切除或转移性滑膜肉瘤患者。
之前我们看到的CAR-T在临床上取得的振奋人心的效果,从分类上来讲,都是在液体瘤中取得的,就是说都是血液癌症。
但Adaptimmune的TCR-T技术目前所有的临床试验,都是在试图攻克固体瘤。
这些Adaptimmune都处于临床1/2期的固体瘤包括卵巢癌,非小细胞肺癌,肝癌,多发性骨髓癌,黑色素瘤等。
Immunocore公司
Immunocore也是一家以TCR-T为只要技术,试图攻破固体瘤的公司。
其目前主要研究的是恶性黑色素瘤的治疗。都在临床1/2期。
Immunocore和Adaptimmnue$(ADAP)$都是以TCR-T为主要技术,研究固体瘤的公司。
目前,人类在攻克癌症上的重大成就都是在血液癌症中取得的,也就是在液体瘤中取得。
但是在像肺癌、肝癌这种更为常见更为致命的“固体瘤”上,我们所取得的进展目前还相当有限。
如果说液体瘤的攻击就像在平原上与癌细胞直接进行短兵相接的话,那么固体瘤的攻击就像攻城拔寨,要攻克一个个城墙堡垒,难度增加很多。
一旦在固体瘤上取得突破性进展,人类攻克癌症的步伐将会向前迈进一大步。
所以对于Immunocore和Adaptimmune这样的公司,临床结果如取得好的成绩,将是非常振奋人心的。 #美股行业分析#






精彩评论