承接上篇,接下来将对$(ARGX)$公司的重磅产品Efgartigimod进行分析与估值。
l Efgartigimod
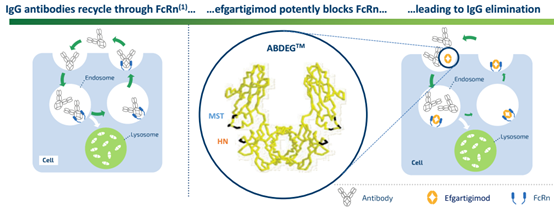
技术原理:全人源抗体,使用了ABDEG,Efgartigimod与FcRn结合而促进病理性的IgG的消除,具体原理如下图。Efgartigimod与FcRn结合的同时,并不与Fcγ受体结合,因而不会招募NK细胞产生ADCC作用。
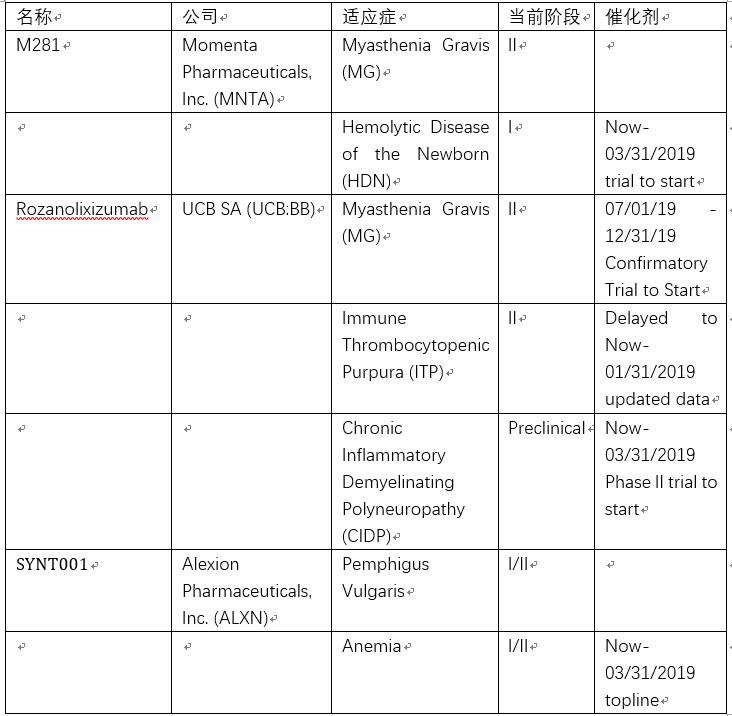
基于相同原理已进入临床阶段的候选药物:
此外,Roivant Sciences, Inc.的RVT-1401正在US之外进行用于Autoimmune Disorders的I期临床试验;Albumedix Ltd.的Albumedix’ Engineered Recombinant Albumins (Veltis)处于临床前,用于肿瘤治疗;Alexion Pharmaceuticals, Inc. (ALXN)还有一款靶向albumin-FcRn interactions 的SYNT002,处于临床前。
(1)Efgartigimod用于重症肌无力(Myasthenia Gravis,MG)
疾病介绍:重症肌无力(Myasthenia Gravis,MG)
重症肌无力(MG)是一种由神经-肌肉接头处传递功能障碍所引起的自身免疫性疾病,临床主要表现为部分或全身骨骼肌无力和易疲劳,活动后症状加重,经休息后症状减轻。患病率为77~150/100万,年发病率为4~11/100万。据估计美国共有64000名MG患者。
重症肌无力的发病原因分两大类,一类是先天遗传性,极少见,与自身免疫无关;第二类是自身免疫性疾病,最常见。发病原因尚不明确,普遍认为与感染、药物、环境因素有关。同时重症肌无力患者中有65%~80%有胸腺增生,10%~20%伴发胸腺瘤。
重症肌无力无法治愈,但可以通过药物治疗,有时也可以通过手术治疗。该病可以首先服用Mestinon增加乙酰胆碱的含量来刺激受体。如果在Mestinon上继续有症状,通常会加一种免疫疗法。这些药物包括硫唑嘌呤(Imuran)、环孢霉素(Neoral)、依库丽单抗(Solaris)、麦考酚脂(CellCept)和强的松(prednisone)来抑制免疫系统。在严重的情况下,可以进行血浆置换。也可以通过静脉针注射静脉注射用免疫球蛋白(IVIg)。如果患者有胸腺瘤,需要手术切除胸腺(胸腺切除术)。事实上,即使没有肿瘤,切除胸腺似乎可以改善许多病人的症状。
竞争情况:
在重症肌无力方向,最新的临床实验数据表明,ARGX-113一周一针的剂量连续注射四针后,在未来一个月的时间内患者体内的IgG下降大约50%。同时,在四个症状测试中,ARGX-113和对照组比都提升了患者的生活质量和减轻了症状。MG-ADL(Myasthenia Gravis Activity of Daily Living)分数的改善度(减小两分,最严重的24分)来看,试验组改善比例为75%,显著高于安慰剂组的25%,p= 0.0391。ARGX-113可用于抗乙酰胆碱受体(AChR)抗体阳性和阴性患者的治疗。入组标准设为MG-ADL(一种用来评估MG严重程度的量表)得分不低于5(满分24,得分越高代表疾病越严重)。
ALXN的Soliris(eculizumab)是最新(2017/10)获批的MG治疗药物,为作用于补体通路的单抗药物,用于治疗抗乙酰胆碱受体(AChR)抗体阳性的全身型重症肌无力(gMG)成年患者。Soliris在临床试验中主要临床试验终点“平均MG-ADL(重症肌无力日常生活质量量表)评分在第26周的变化”并未作出显著性差异(0.1>p>0.05)。入组标准为MG-ADL得分不低于6(满分24)。
据以上信息,ARGX-113可能具有不逊于Soliris的治疗效果。AChR抗体阳性的MG患者约为全部MG患者的80%-90%,ARGX-113的适应人群略多于Soliris。又从作用机理来说,ARGX-113通过减小IgG的半衰期来减缓症状,副作用应该比现有疗法都要小。临床数据也证实,ARGX-113目前只会在病人体内出现1-2级的AE(Adverse Effect)。
UCB SA 的Rozanolixizumab目前已取得II期的top-line结果。该药与ARGX-113的作用机制相同。在II期试验中,1阶段结束后MG-ADL得分试验组平均降低2个点、安慰剂组0.18点,P=0.008;在MGC和QMG方面,没有做出显著性差异,p>0.1。该试验入组标准为QMG(一种用来评估MG严重程度的量表)得分不低于11(满分39,得分越高代表疾病越严重)。按照11/39和5/24计算,ARGX-113入组的患者更为轻些。据此综合来看,ARGX-113的治疗效果略好于Rozanolixizumab。不过Rozanolixizumab给药渠道给SQ,好于ARGX-113当前的静脉给药。
M281与ARGX-113的作用机制相同,II期试验于2018年12月10日启动,显著慢于ARGX-113和Rozanolixizumab。
目前还有CPRX的钾离子通道阻断剂Firdapse用来治疗MuSK抗体阳性的MG,临床III期结果数据非常好,在多项量表中均表现出显著好于安慰剂的疗效,MG-ADL参数的p值为0.0006。MuSK抗体阳性患者占MG患者的比例约为5-8%。
估值分析:
Soliris目前被FDA获批了包括MG在内的三个适应症。美国市场,2017年(MG适应症刚获批)销售额为12.35亿美元,较上年增速为16.7%;2018年前九个月销售额较上年同期增加24.4%;2018年第三季度销售额较上年同期增加31%。据此,粗略计算2018年的总销售额较2017年增加约24.4%,其中由MG贡献的销售额预计为0.95亿美元。按照Soliris用于MG的年花费(Wholesale price)为70万美元,据此估计当前使用的患者人数为184人,占所有MG患者的0.3%。保守按峰值销售额为首年销售额的8倍(经验值,此时患者人数占MG患者的2.4%,数值合理)计算,Soliris在MG上的巅峰销售额约为7.6亿美元。
从作用机制来看,可能与Soliris有竞争但不是完全的替代关系。合理地估计定价与Soliris相当,可能巅峰销售额与Soliris在MG适应症下的销售额相同,保守估计巅峰销售额为4.5亿美元。
ARGX-1132018年9月启动III期临床,假设能在2022年获批,预计2027年达到巅峰销售额。市销率设为3,ARGX-113在该适应症下的美国市场保守估计价值5.85亿美元。
(2)Efgartigimod用于原发免疫性血小板减少症(ITP)
疾病介绍:原发免疫性血小板减少症(ITP),以往称特发性血小板减少性紫癜,是一种获得性自身免疫性疾病。ITP在各个年龄阶段均可发病,一般儿童多为急性型,成人多为慢性型。两种类型在发病年龄、病因、发病机制及预后有所不同。80%以上儿童患者不管治疗与否,近半数患者在6周内血小板计数恢复正常,只有少部分转为慢性ITP。成人ITP自发缓解者很少,约1/3患者对糖皮质激素及脾切除治疗无效,迁延不愈,但大多数预后良好,死亡率并不比一般人群高,约5%患者死于颅内出血。预计全美ITP患者人数约为65000人,与MG的人数基本相同。
治疗药物包括:
糖皮质激素:是治疗ITP的首选药物。适用血小板计数<30×10/L,并且有严重出血;或出血危险者;或存在明显的乏力症状者。一般口服首选泼尼松。治疗有效后逐渐减量直至停药。
大剂量静脉丙种球蛋白:在有紧急出血情况时应用,副作用轻微。
脾切除:脾切除被认为是仅次于糖皮质激素的主要治疗方法。用于糖皮质激素治疗无效或剂量依赖者。有效率在60%~80%。
其他免疫抑制剂:包括达那唑、长春新碱、环磷酰胺、环孢素A、硫唑嘌呤等。对慢性ITP经糖皮质激素或脾切除治疗疗效不佳者,或者不适宜糖皮质激素、脾切除治疗者可采用其中单一药物治疗或联合方案治疗。
血小板生成素受体激动剂:是与发病机制研究成果相关的治疗理念的更新。包括血小板生成素(TPO)、TPO拟肽和非拟肽类TPO类似物。此类药物耐受性良好,不良反应轻微。
利妥昔单抗(rituximab、抗CD20单抗、美罗华):可抑制生成抗血小板自身抗体的异常B细胞。使ITP获得长期持续缓解,但起效较慢、价格较昂贵。
竞争分析:
根据现有的试验方案,ARGX-113主要用于慢性ITP(过去4周较为稳定)的治疗,要求平均血小板技术不高于30 × 109/L。
在免疫性血小板减少症(Immune Thrombocytopenia, ITP)的临床2期数据,疗效没有那么理想。虽然IgG的血液浓度和血小板数在病人中显示出明显的负相关,有46%的病人注射后血小板计数达到了临床显著改善的水平(>50*10E9/L),只有38%的病人在血小板计数上有持续超过10天的显著改善。
估值分析:
Romiplostim和Eltrombopag, 作为ITP治疗的最后一线药物,2016年全球销售额分别为5.84亿美元和6.35亿美元。根据ITP病人基数和重症肌无力人数差不多,疗效可能不佳,但用药次数2-3次高于MG的单次用药(III期试验方案),预计在单次给药10万美元的基础上,也能达到MG上的巅峰销售额4.5亿美元水平。
ARGX-113当前未开始III期临床,假设能在2025年获批。预计2030年达到巅峰销售额。市销率设为3。ARGX-113在该适应症下美国市场价值为:1.74亿美元。
(3)Efgartigimod用于其它适应症
Pemphigus Vulgaris适应症美国病人总数为30000-40000人。当前处于临床II期,获批可能性为20% (Same As Avg.),预计Now-06/30/19最终数据。
Chronic Inflammatory Demyelinating Polyneuropathy (CIDP)适应症预计Now-06/30/19启动II期临床。
两个适应症打包美国市场价值设为1.74亿美元。
Efgartigimod在美国市场的估值合计为9.33亿美元,考虑欧洲市场,粗略预计总市场规模为14亿美元。
下篇将对ARGX公司的另一个重磅产品ARGX-110进行分析与估值,并对公司的财务状况进行分析,给出投资建议,尽请期待。
免责声明
报告的全部内容只供做参考之用,并不构成投资建议,也并非作为买卖、认购股票或其它金融工具的保证。基岩研究院对这些信息的准确性和完整性不作任何保证,也不保证所包含的信息和建议不会发生任何变更。投资者依据本报告提供的信息进行证券投资所造成的一切后果自负。
精彩评论