近日,美国血液学会(ASH)年会召开,作为全球血液学领域最负盛名的国际学术盛会之一,能够在ASH年会上发布临床数据的产品无疑都具备显著的创新性和临床应用潜力,同时也反映了企业在创新研发方面的实力。
会上,基石药业公布了重磅产品CS5001作为单药针对晚期淋巴瘤的最新临床数据,展现出良好的疗效和安全性。作为首个在实体瘤和淋巴瘤中均观察到临床疗效的ROR1 ADC,CS5001的亮相快速引起了业内的广泛关注。
公告一经发出,基石药业的股价涨幅一度超过7%,可见市场对该产品前景的积极反应。对于投资者而言,这背后或许也隐藏着一个有价值的投资机会。
1、ORR高达76.9%,潜在同类最佳彰显差异化临床价值
从产品结构设计上来看,CS5001作为一种新型ROR1导向的ADC,就已经展现出十足的创新性。吡咯并苯二氮卓(PBD)前药的独特设计,赋予了CS5001拥有同类最佳产品潜力的优势。简单来说有四大差异化优势:
其一,全人源抗IgG1抗ROR1抗体因其与人体的高度相容性而减少免疫原性,从而可能降低副作用风险,提高治疗安全性;
其二,位点特异性偶联技术能够精确控制药物与抗体的比例达到2,有助于确保药物的均匀分布和稳定性,提高疗效并减少副作用;
其三,专属肿瘤选择性可降解连接子(由β-葡萄糖醛酸酶裂解)意味着其能够在血液循环系统中保持高度稳定,直到到达肿瘤微环境;
其四,肿瘤微环境中特异性激活PBD二聚体毒素前药(由β-葡萄糖醛酸酶酶切释放)能够通过DNA交联机制有效杀伤肿瘤细胞,避免肿瘤耐药性的产生。
基于此,本次CS5001作为单药针对晚期淋巴瘤最新的积极临床数据,也进一步证明了CS5001的安全性和潜在的临床应用价值。
于疗效性方面,无论患者的ROR1表达水平如何,从最低有效剂量开始,CS5001在晚期霍奇金淋巴瘤(HL)患者中的ORR达到了60.0%,而在非霍奇金淋巴瘤(NHL)患者中的ORR为56.3%。
特别值得一提的是,在初步确定的II期推荐剂量(RP2D)水平——DL8(125 μg/kg)中,晚期B细胞淋巴瘤患者的ORR更是高达76.9%,其中所有可评估的HL患者均实现了完全或部分缓解,NHL患者的ORR也达到了70%。
于安全性方面,CS5001在多线经治的晚期B细胞淋巴瘤患者中,展现出良好的耐受性,且在10个不同剂量组的研究中,没有报告任何剂量限制性毒性(DLT)。
进一步对比市场上已有的两种相关ADC,CS5001在I期临床试验中的不良事件发生率相对较低。特别是在I期剂量探索研究中,与其他PBD类ADC相比,CS5001也显示出更低的血液学毒性。
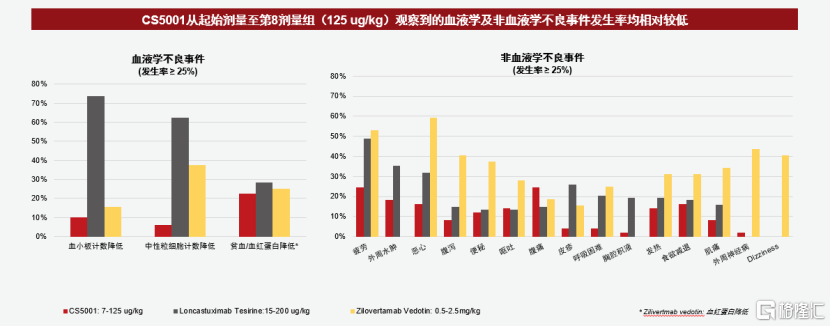
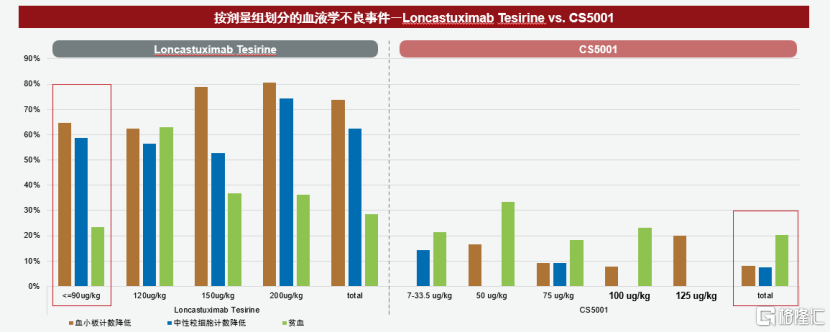
随着CS5001在临床试验中展现出的积极数据,我们有理由相信,ROR1 ADC药物有望成为全球晚期淋巴瘤患者治疗的重要选择。
据悉,目前CS5001的全球多中心试验正在美国、澳大利亚和中国同步进行,剂量递增阶段已经顺利完成,该产品的国际化步伐正在稳步推进,并且基石药业还将于近期启动涵盖多瘤种、具有注册潜力的1b期剂量扩展研究。
可以预见,此次针对晚期淋巴瘤治疗的积极结果,也将为CS5001在其他多种实体瘤和血液瘤的探索上提供经验和数据支撑,展现出更多临床应用潜力。
2、手握多款FIC/BIC,增长引擎正在加速转动
透过CS5001,背后映射出来的则是基石药业的创新能力。
从管线布局来看,基石药业2.0的管线主打差异化竞争,PD-1/VEGFA/CTLA4三抗、EGFR/HER3双抗及ADC、ITGB4 ADC、SSTR2系列管线,自免双抗管线等17款候选药物极具市场潜力,致力于最大化成熟产品的商业价值。

除了此次ASH年会上公布数据的CS5001外,基石药业的CS2009也是一大值得关注的亮点。
作为PD-1/VEGFA/CTLA-4三特异性抗体,CS2009独特的设计有望使其取代现有的PD-(L)1单抗,成为下一代肿瘤免疫治疗的骨干产品,具有成为FIC的潜力,目前即将进入临床阶段。
最新的临床数据显示,与PD-1/L1单药治疗相比,PD-1/L1联合VEGFA治疗虽然能够改善无进展生存期(PFS),但在总生存期(OS)上的获益并不明显。同时,PD-1/L1联合CTLA-4治疗的长期生存协同作用在最近发表的临床数据中得到了证实。
基于这些发现,基石药业通过将PD-1、VEGFA和CTLA-4三种抗体联合起来,旨在实现最大的生存获益。此前,CS2009的临床前研究数据就已经显示出在抗肿瘤活性方面明显优于潜在的竞品,包括PD-1/CTLA-4双抗和PD-1/VEGFA双抗。
值得注意的是,基石药业也是推动中国生物药国际化的排头兵,旗下已有3款商业化产品通过合作伙伴在全球市场销售。此外,首个成功出海的由中国生物制药企业研发的PD-L1单抗——舒格利单抗目前已获得在欧盟,欧洲经济区国家以及英国的上市许可。毫无疑问,这将为基石药业未来其他产品的上市和国际市场开拓提供有力的支持和快速的放量。
根据今年的中期业绩报告,基石药业现已开始盈利,进一步印证了其的增长引擎正在良性转动。强势的临床开发能力结合差异化的产品管线,国内自主开发与全球商业化合作并行,基石药业已经具备了中国Biotech可持续发展的核心要素。相信随着公司对创新管线研发的持续深入,会陆续收获市场价值的回馈。
精彩评论